
下列敘述正確的是
A.K+、ClO‐、SO42‐、HCO3‐一定能共存于 c(Fe3+)=0.1mol·L‐l 的溶液中
B.磁性氧化鐵(Fe3O4)溶于氫碘酸: Fe3O4+8H+=Fe2++2Fe3++4H2O
C.在NaClO和NaCl混合溶液中通入過量SO2氣體,反應的離子方程式為:SO2+3C1O‐+H2O=SO42‐+C1‐+2HClO
D.均為0.1mol/L Na+、HCO3-、Br-、Mg2+可以在 pH=8 的溶液中共存 Ksp(Mg(OH)2)=1.0×10-11
 金牌教輔培優優選卷期末沖刺100分系列答案
金牌教輔培優優選卷期末沖刺100分系列答案科目:高中化學 來源:2017屆江西省高三上月考五化學試卷(解析版) 題型:選擇題
室溫下,將1 mol的CuSO4·5H2O(s)溶于水會使溶液溫度降低,熱效應為ΔH1,將1 mol的CuSO4(s)溶于水會使溶液溫度升高,熱效應為ΔH2;CuSO4·5H2O受熱分解的化學方程式為CuSO4·5H2O(s) 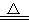 CuSO4(s)+5H2O(l),熱效應為ΔH3,則下列判斷正確的是( )
CuSO4(s)+5H2O(l),熱效應為ΔH3,則下列判斷正確的是( )
A.ΔH2>ΔH3 B.ΔH1+ΔH3=ΔH2 C.ΔH1<ΔH3 D.ΔH1+ΔH2>ΔH3
查看答案和解析>>
科目:高中化學 來源:2016-2017學年陜西省高二上期中化學卷(解析版) 題型:填空題
2016年10月17日我國神舟十一號載人飛船在酒泉衛星發射中心成功發射,為我們更好地掌握空間交會對接技術、開展地球觀測活動奠定了基礎。我國制造航天飛船的主要材料是鋁,因而其也被稱為會飛的金屬,請根據其性質回答下列問題:
(1)現在工業冶煉鋁的化學方程式為 。
(2)鋁鋰合金是今年來航空金屬材料中發展最為迅速的一個領域,主要因為合金的某些性能優于各成分金屬,其中包括 、 等方面。同時鋁鋰形成化合物LiAlH4既是金屬儲氫材料又是有機合成中的常用試劑,遇水能得到無色溶液并劇烈分解釋放出H2,LiAlH4在化學反應中通常作
(填“氧化”或“還原”)劑。
(3)鋁電池性能優越,在現代生產、生活中有廣泛的應用。
①Al-Ag2O電池可用作水下動力電源,化學反應為2Al+3Ag2O+2NaOH=2NaAlO2+6Ag+H2O,則負極的電極反應式為 ,正極附近溶液的pH (填“變大”“不變”或“變小”),
②鋁一空氣電池以其環保、安全而受到越來越多的關注,其原理如下圖所示。

該電池的負極反應方程式為 ;正極反應方程式為 ;
電池中NaCl溶液的作用是 ;以該電池為電源,用惰性電極電解Na2SO4溶液,當Al電極質量減少1.8g時,電解池陰極生成的氣體在標準狀況下的體積為 L。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年陜西省高二上期中化學卷(解析版) 題型:選擇題
25℃時,在飽和氯水中存在平衡:Cl2+H2O H++Cl-+HClO,下列敘述中正確的是( )
H++Cl-+HClO,下列敘述中正確的是( )
A.用pH試紙測得溶液pH<7
B.向其中加入AgNO3溶液,平衡向右移,溶液的pH變小
C.向其中加入NaOH使pH=7,所得溶液中微粒濃度的關系如下:c(Na+)>c(Cl-)>c(ClO-)=c(HClO)
D.若氯水久置pH會逐漸增大
查看答案和解析>>
科目:高中化學 來源:2017屆天津市高三上月考三化學試卷(解析版) 題型:填空題
重鉻酸鉀是一種常見的強氧化劑。實驗室以精選鉻鐵礦(主要成分可表示FeO·Cr2O3,還含有 SiO2、 Al2O3 等雜質)為原料制備重鉻酸鉀晶體(K2Cr2O7,式量294)的流程如下:
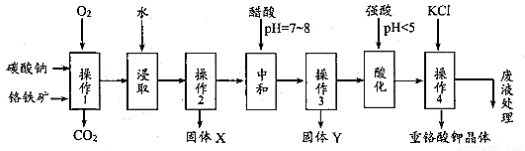
請回答下列問題:
操作1中發生的反應有:
4FeO·Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2↑;
8Na2CrO4+2Fe2O3+8CO2↑;
Na2CO3+Al2O3 2NaAlO2+CO2↑;Na2CO3+SiO2
2NaAlO2+CO2↑;Na2CO3+SiO2 Na2SiO3+CO2↑
Na2SiO3+CO2↑
該步驟在常溫下的反應速度較慢,為使反應速率增大,可采取的兩條措施是____________。
(2)固體Y 中主要含有______________。(填寫化學式)
(3)酸化步驟使含鉻物質發生了轉化,請寫出離子反應方程式______________________。
(4)操作 4 中的化學反應在溶液中能發生的可能理由是_________________________;獲得 K2Cr2O7 晶體的操作依次是:加入KCl 固體,在水浴上加熱濃縮至______________,冷卻結晶,抽濾,洗滌,干燥。
(5)通過下列實驗可測定產品中重鉻酸鉀的質量分數:稱取重鉻酸鉀試樣 1.470g,用100mL 容量瓶配制成溶液。移取25.00mL 溶液于碘量瓶中,加入適里稀硫酸和足量碘化鉀(鉻的還原產物為 Cr3+),放于暗處 5min。然后加入一定量的水,加入淀粉指示劑,用0.1500mol/L 標準溶液滴定,共消耗標準液36.00mL。滴定時發生的反應的離子方程式為:I2+2S2O32-=2I-+S4O62-;則所測產品中重鉻酸鉀的純度為_____________。
(6)有關上述實驗過程中涉及的部分實驗操作的描述,正確的是_________.
A.粗產品若要進一步提純,可以采用重結晶的方法
B. 配制溶液時,用托盤天平稱取試樣后,一般經溶解、轉移(含洗滌)、定容等步驟,配制成100mL溶液
C.滴定時,當最后一滴標準溶液滴入時,溶液變為藍色,且半分鐘內不變色,可判斷滴定終點
D.滴定終點時俯視讀數,測定結果偏低
查看答案和解析>>
科目:高中化學 來源:2017屆寧夏高三上月考五化學試卷(解析版) 題型:填空題
【化學——選修物質結 構與性質】主族元素碳、氧、氮、氟、磷、硒及副族元素鎳、銅元素在化學中有很重要的地位,回答下列問題:
構與性質】主族元素碳、氧、氮、氟、磷、硒及副族元素鎳、銅元素在化學中有很重要的地位,回答下列問題:
(1)在基態14C原子中,核外存在 對自旋相反的電子,基態氮原子的價層電子排布圖為_________________________。
(2)將F2通入稀NaOH溶液中可生成OF2,OF2分子構型為 ,其中氧原子的雜化方式為 。
(3)過渡金屬配合物Ni(CO)n的中心原子價電子數與配體提供電子總數之和為18,則n= 。CO與N2結構相似,CO分子內σ鍵與π鍵個數之比為 。
(4)CuSO4溶液能用作P4中毒的解毒劑,反應可生成P的最高價含氧酸和銅,該反應的化學方程式是 。
(5)H2SeO3的K1和K2分別為2.7×10-3和2.5×10-8,H2SeO4第一步幾乎完全電離,K2為1.2×10-2,請根據結構與性質的關系解釋H2SeO4比H2SeO3酸性強的原因: ;
(6)已知Cu2O為半導體材料,在其立方晶胞內部有4個氧原子,其余氧原子位于面心和頂點,則該晶胞中有 個銅原子。
(7)用晶體的X射線衍射法對Cu的測定得到以下結果:Cu的晶胞為面心立方最密堆積(如右圖),已知該晶體的密度為9.00 g·cm-3,Cu的原子半徑為________cm(阿伏加德羅常數為NA,只要求列式表示)。
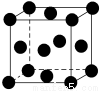
查看答案和解析>>
科目:高中化學 來源:2017屆寧夏高三上月考五化學試卷(解析版) 題型:選擇題
某電池是一種新型可充電電池,與普通高能電池相比,該電池能長時間保持穩定的放電電壓。該電池是以K2FeO4和Zn為電極材料,KOH溶液為電解 溶質溶液,其總反應為:3Zn+2K2FeO4+8H2O
溶質溶液,其總反應為:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列說法正確的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列說法正確的是
A.Zn為電池的正極
B.充電時陽極反應為:Fe(OH)3-3e?+5OH? =FeO42-+4H2O
C.放電時每轉移3 mol電子,正極有1 mol K2FeO4被氧化
D.該電池放電過程中電解質溶液濃度不變
查看答案和解析>>
科目:高中化學 來源:2017屆寧夏高三上月考二化學卷(解析版) 題型:選擇題
用下圖所示實驗裝置進行相應實驗,能達到實驗目的的是

A.用圖①所示裝置,蒸干NH4Cl飽和溶液制備NH4Cl晶體
B.按裝置②所示的氣流方向可用于收集H2、NH3等
C.用圖④所示裝置,分離CCl4萃取I2水后的有機層和水層
D.用圖④所示裝置,可以證明氧化性Cl2>Br2>I2
查看答案和解析>>
科目:高中化學 來源:2016-2017學年吉林長春外國語學校高一上期末文化學卷(解析版) 題型:選擇題
在實驗室中,要想使AlCl3溶液中的Al3+全部沉淀出來,應選用下列試劑中
A、石灰水 B、氫氧化鈉溶液 C、硫酸 D、氨水
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com