

| 物質 | 熔點/℃ | 沸點/℃ |
| 1-丁醇 | -89.5 | 117.3 |
| 1-溴丁烷 | -112.4 | 101.6 |
| 丁醚 | -95.3 | 142.4 |
| 1-丁烯 | -185.3 | -6.5 |
分析 (1)裝置圖分析冷凝回流的主要目的是提高反應物的利用率;
(2)理論上,上述反應的副產物可能有:丁醚(CH3CH2CH2CH2-O-CH2CH2CH2CH3)、1-丁烯、溴化氫、硫酸氫鈉、水等,能通過裝置BC檢出的是氣體應檢驗1-丁烯、溴化氫的存在,先檢驗溴化氫的存在用石蕊試液或硝酸銀溶液檢驗,后檢驗1-丁烯,選擇試劑為溴水或高錳酸鉀溶液褪色驗證;C裝置中主要的1-丁烯和溴單質發生加成反應;
(3)提純1-溴丁烷,收集所得餾分為1-溴丁烷,所以須將1-溴丁烷先汽化,后液化,汽化須溫度達其沸點101.6℃,需要理由蒸餾裝置可知溫度,冷卻等操作規程設計步驟;
(4)依據化學方程式分析1-丁醇、NaBr反應情況,依據化學方程式計算生成的1-溴丁烷質量,依據產率=$\frac{實際量}{理論量}$×100%計算得到.
解答 解:(1)關閉a和b、接通豎直冷凝管的冷凝水,進水口為Ⅱ;給A加熱30分鐘,制備1-溴丁烷.冷凝回流的主要目的是,充分利用反應物,提高反應物的轉化率,
故答案為:Ⅱ;充分反應,提高反應物的轉化率;
(2)理論上,上述反應的副產物可能有:丁醚(CH3CH2CH2CH2-O-CH2CH2CH2CH3)、1-丁烯、溴化氫、硫酸氫鈉、水等,能通過裝置B、C裝置檢出的是氣體,應檢驗1-丁烯、溴化氫的存在,先檢驗溴化氫的存在用石蕊試液或硝酸銀溶液檢驗,通過石蕊試液溶液變紅色(通過硝酸銀溶液生成淺黃色沉淀)證明溴化氫的生成;后檢驗1-丁烯,選擇試劑為溴水或高錳酸鉀溶液,通過為溴水或高錳酸鉀溶液褪色證明生成的產物中含有1-丁烯,C裝置中主要的化學方程式CH3CH2CH=CH2+Br2→BrCH2CHBrCH2CH3 ;
故答案為:石蕊試液(或AgNO3溶液);溴水(或酸性KMnO4溶液);CH3CH2CH=CH2+Br2→BrCH2CHBrCH2CH3 ;
(3)提純1-溴丁烷,收集所得餾分為1-溴丁烷,所以須將1-溴丁烷先汽化,后液化,汽化須溫度達其沸點101.6℃,利用蒸餾原理和裝置設計的步驟為:
①待燒瓶冷卻后,拔去豎直的冷凝管,②插上帶橡皮塞的溫度計 ③關閉a,打開b ④接通冷凝管的冷凝水,使冷水從d處流入 ⑤迅速升高溫度至101.6℃;通過蒸到分離、提純1-溴丁烷,
故答案為:關閉a,打開b;
(4)若實驗中所取1-丁醇、NaBr分別為7.4g、13.0g,依據化學方程式計算判斷反應情況:
CH3CH2CH2CH2OH+NaBr+H2SO4$\stackrel{△}{→}$CH3CH2CH2CH2Br+NaHSO4+H2O
74 103
7.4g 10.3g
溴化鈉過量,則1-丁醇全部反應生成1-溴丁烷物質的量為0.1mol,質量=0.1mol×137g/mol=13.7g;
蒸出的粗產物經洗滌、干燥后再次蒸餾得到9.6g 1-溴丁烷,產率=$\frac{9.6g}{13.7g}$×100%=70%,
故答案為:70%.
點評 本題主要考查了1-溴丁烷的制取實驗,混合物分離的實驗操作步驟和過程分析判斷,明確反應原理是解答的關鍵,題目難度中等.


 王后雄學案教材完全解讀系列答案
王后雄學案教材完全解讀系列答案 海淀課時新作業金榜卷系列答案
海淀課時新作業金榜卷系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
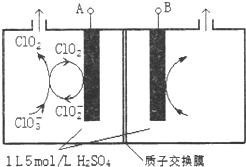 二氧化氯(ClO2)是國內外公認的高效、廣譜、快速、安全無毒的殺菌消毒劑,被稱為“第4代消毒劑”.工業上可采用氯酸鈉(NaClO3)或亞氯酸鈉(NaClO2)為原料制備ClO2.
二氧化氯(ClO2)是國內外公認的高效、廣譜、快速、安全無毒的殺菌消毒劑,被稱為“第4代消毒劑”.工業上可采用氯酸鈉(NaClO3)或亞氯酸鈉(NaClO2)為原料制備ClO2.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 綠色食品是指不含任何化學物質的食品 | |
| B. | 苯主要是從石油分餾而獲得的一種重要化工原料 | |
| C. | 煤經氣化和液化兩個化學變化過程可以轉變為清潔能源 | |
| D. | 乙烯和苯均能發生氧化反應,說明兩者都有碳碳雙鍵 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com