
| 步驟 | 操作 | 甲組現象 | 乙組現象 |
| 1 | 取黑色粉末加入稀鹽酸 | 溶解,無氣泡 | 溶解,有氣泡 |
| 2 | 取步驟1中溶液,滴加KSCN溶液 | 變紅 | 無明顯變化 |
| 3 | 向步驟2溶液中滴加新制氯水 | 紅色先變深后褪去 | 先變紅后也褪色 |
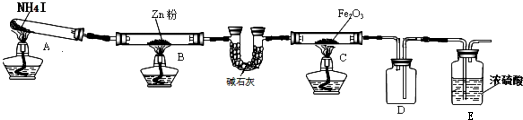
分析 裝置A中碘化銨加熱分解,實驗時A中有大量紫紅色的煙氣,得到碘單質、氨氣、氫氣、碘化氫等,通過裝置B中 的鋅加熱反應吸收碘蒸氣生成ZnI2,剩余氣體通過堿石灰吸收水蒸氣和HI,進入裝置C中玻璃管加熱氫氣還原氧化鐵反應,生成的氣體進入裝置D是安全瓶,防止倒吸,最后進入裝置E的濃硫酸吸收多余的氨氣,
(1)實驗時中A有大量紫紅色的煙氣,說明生成了碘蒸氣,NH4I發生下列反應:NH4I(固)?NH3(氣)+HI(氣),2HI(氣)?H2(氣)+I2(氣),則NH4I的分解產物為 NH3、H2、I2(HI),E裝置濃硫酸的作用是 吸收多余的氨氣,堿石灰是吸收水蒸氣和酸性氣體;
(2)裝置B中鋅的作用是吸收碘蒸氣,反應方程式:Zn+I2═ZnI2,故D裝置的作用是作安全瓶,防倒吸,因為氨氣極易被濃硫酸吸收;
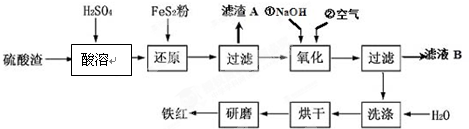
(3)利用黑色固體可溶于鹽酸并產生氣體,結合“原子守恒”可知用酒精噴燈的乙組實驗得到的固體為Fe;
(4)Fe2O3被還原得到黑色固體為Fe3O4,由此可寫出反應的離子方程式;
(5)步驟4中溶液變紅是溶液中Fe2+被Cl2氧化為Fe3+所致、溶液褪色的原因可能是Cl2將SCN-氧化;
(6)氧化物樣品質量為7.84克,還原成鐵粉質量為5.6克,設出氧化鐵和氧化亞鐵的物質的量,分別根據鐵的質量、總質量列式計算即可.
解答 解:(1)實驗時中A有大量紫紅色的煙氣,說明生成了碘蒸氣,NH4I發生下列反應:NH4I(固)?NH3(氣)+HI(氣),2HI(氣)?H2(氣)+I2(氣),則NH4I的分解產物為 NH3、H2、I2(HI),堿石灰是吸收水蒸氣和酸性氣體,
故答案為:NH3、H2、I2(HI);干燥及吸收酸性氣體;
(2)裝置B的作用是吸收碘蒸氣,反應方程式:Zn+I2═ZnI2,因為氨氣極易被濃硫酸吸收,故D裝置的作用是作安全瓶,防倒吸,
故答案為:Zn+I2═ZnI2;安全瓶;
(3)利用黑色固體可溶于鹽酸并產生氣體,結合“原子守恒”可知用酒精噴燈的乙組實驗得到的固體為Fe,故答案為:Fe;
(4)利用甲組現象可知Fe2O3與CO在酒精燈加熱的條件下,Fe2O3被還原得到黑色固體為Fe3O4,由此可寫出反應的離子方程式為Fe3O4+8H+=2Fe3++Fe2++4H2O,
故答案為:Fe3O4+8H+=2Fe3++Fe2++4H2O;
(5)因Fe3+遇SCN-顯紅色,所以乙組步驟3中溶液變紅是溶液中Fe2+被Cl2氧化為Fe3+所致,溶液褪色的原因可能是Cl2將SCN-氧化,
故答案為:Fe2+被氧化為Fe3+,Fe3+遇SCN-顯紅色;
(6)設氧化鐵的物質的量為x,氧化亞鐵的物質的量為y,則:160x+72y=7.84、(2x+y)×56=5.6,
聯立解得:x=0.04mol、y=0.02mol,
則混合物中Fe2O3和FeO的物質的量之比為:0.04mol:0.02mol=2:1,
故答案為:2:1.
點評 本題考查了鐵離子、亞鐵離子的檢驗方法、性質實驗方案的設計與評價,題目難度中等,試題綜合性較強,注意正確理解、分析題中信息,聯系所學的知識進行解答.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | K+和Na+ | B. | Al3+和Cl- | C. | OH-和NH4+ | D. | H2S和CH4 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 開始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
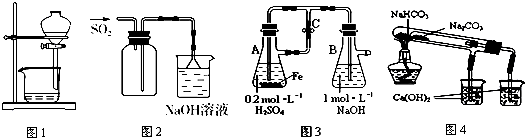
| A. | 圖1用于放出碘的苯溶液 | |
| B. | 圖2用于實驗室收集SO2 | |
| C. | 圖3用于實驗室制備Fe(OH)2 | |
| D. | 圖4用于比較NaHCO3和Na2CO3熱穩定性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溫度相同、體積相同的O2和N2 | B. | 質量相等、密度不等的N2和C2H4 | ||
| C. | 體積相同、密度相等的CO和N2O | D. | 壓強相同、體積相同的O2和H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | B的陽離子的氧化性比A的陽離子強,則A元素的金屬性不一定比B元素強 | |
| B. | 發生氧化還原反應時,A原子失去的電子比B原子多,證明A的金屬性一定比B強 | |
| C. | 適量的Cl2通入FeI2溶液中可發生反應:3Cl2+6FeI2═2FeCl3+4FeI3 | |
| D. | A的金屬性比B的金屬性強,則A一定可以在水溶液置換出B來 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com