
| A. | 四項 | B. | 三項 | C. | 二項 | D. | 一項 |
分析 ①元素化合價的絕對值+該元素原子最外層電子數=8,元素原子滿足8電子結構;
②分子晶體的堆積不一定是分子密堆積,如冰晶體中存在氫鍵,不是分子密堆積;
③NaCl晶胞結構為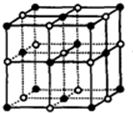 ,晶體中與每個Na+距離相等且最近的Na+個數=3×8÷2;
,晶體中與每個Na+距離相等且最近的Na+個數=3×8÷2;
④稀有氣體單質不存在任何化學鍵;
⑤分子晶體由固體變為氣體,克服分子間作用力;
⑥晶體有自范性,而非晶體沒有,單晶體各向異性,多晶體則為各向同性;
⑦SiC晶胞與金剛石一樣;
⑧中心原子采取sp3雜化的分子,VSEPR模型是正四面體,但其立體構形不一定是正四面體.
解答 解:①NCl3分子中N元素化合價為-3,N原子最外層電子數為5,所以3+5=8,N原子達8電子結構;Cl元素化合價為+1價,F原子最外層電子數為7,1+7=8,Cl原子滿足8結構,故①錯誤;
②分子晶體的堆積不一定是分子密堆積,如冰晶體中存在氫鍵,不是分子密堆積,故②錯誤;
③NaCl晶胞結構為 ,NaCl晶體中與每個Na+距離相等且最近的Na+個數=3×8÷2=12,故③正確;
,NaCl晶體中與每個Na+距離相等且最近的Na+個數=3×8÷2=12,故③正確;
④稀有氣體單質不存在任何化學鍵,故④錯誤;
⑤分子晶體由固體變為氣體,克服分子間作用力,C60、I2均為分子晶體,則C60氣化和I2升華克服的作用力相同,故⑤正確;
⑥晶體的規則幾何外形是自發形成的,有些固體盡管有規則的幾何外形,但由于不是自發形成的,所以不屬于晶體,所以晶體具有自范性,非晶體沒有自范性,但單晶體各向異性,多晶體和非晶體則為各向同性,所以不能用各向異性來區分晶體和非晶體,故⑥錯誤;
⑦SiC晶胞與金剛石一樣,所以1個SiC晶胞中一共有8個原子,故⑦錯誤;
⑧中心原子采取sp3雜化的分子,VSEPR模型是正四面體,但其立體構形不一定是正四面體,如:水和氨氣分子中中心原子采取sp3雜化,但H2O是V型,NH3是三角錐型,故⑧正確;
故選B.
點評 本題考查晶體類型與結構、性質等,難度不大,注意基礎知識的掌握與晶體中的特殊性.


 中考利劍中考試卷匯編系列答案
中考利劍中考試卷匯編系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C2H5OH在電池的負極上參加反應 | |
| B. | 在外電路中電子由負極沿導線流向正極 | |
| C. | 1 mol乙醇被氧化轉移6 mol電子 | |
| D. | 電池正極得電子的物質是O2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在一個基態多電子的原子中,不可能有兩個能量完全相同的電子 | |
| B. | 金屬Na、Mg、Al的硬度依次降低 | |
| C. | 由原子間通過共價鍵而形成的晶體一般具有高的熔、沸點及硬度 | |
| D. | PCl3和CO32-的中心原子的雜化方式相同,都是sp3雜化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
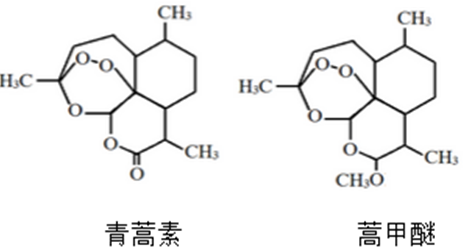
| A. | 蒿甲醚的相對分子質量為295 | |
| B. | 蒿甲醚結構中含有兩個酯基 | |
| C. | 二者互為同分異構體 | |
| D. | 二者均既具有氧化性,又具有還原性 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 如圖為某種燃料電池的工作原理示意圖,a、b 均為惰性電極.
如圖為某種燃料電池的工作原理示意圖,a、b 均為惰性電極.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Mg電極是該電池的正極 | |
| B. | 電池工作時實現了電能向化學能的轉化 | |
| C. | H2O2在石墨電極上發生還原反應 | |
| D. | 電子從石墨電極流向Mg電極 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com