
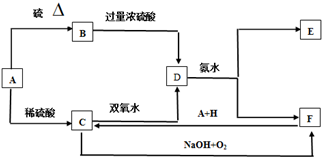
分析 由將D溶液滴入沸水中可得到以F為分散質的紅褐色液體,說明F為Fe(OH)3;證明D為硫酸鐵,E為硫酸銨;由轉化關系可知,C為硫酸亞鐵,轉化關系中A和硫酸反應和硫單質加熱反應,說明A為金屬單質,轉化關系中F(Fe(OH)3)+H+A(Fe)=C(FeSO4),推斷A為Fe,B為FeS,H為硫酸,C為硫酸亞鐵,被過氧化鈉氧化為D硫酸鐵,根據判斷出的物質回答問題.
解答 解:將D溶液滴入沸水中可得到以F為分散質的紅褐色液體,說明F為Fe(OH)3;證明D為硫酸鐵,E為硫酸銨;由轉化關系可知,C為硫酸亞鐵,推斷A為Fe;B為FeS,轉化關系中F(Fe(OH)3)+H+A(Fe)=C(FeSO4),推斷H為硫酸;根據判斷出的物質回答問題:綜上所述各物質為:A、Fe;B、FeS;C、FeSO4;D、Fe2(SO4)3;E、(NH4)2SO4;F、Fe(OH)3;H、H2SO4;
(1)紅褐色液體是氫氧化鐵膠體,分散質粒子直徑大小的范圍是1nm-100nm,
故答案為:1nm-100nm;
(2)依據推斷可知A為Fe,B的化學式為:FeS,H為H2SO4;
故答案為:Fe;FeS;H2SO4;
(3C的酸性溶液與雙氧水反應,是FeSO4的溶液(A→C稀硫酸過量)與雙氧水在酸性溶液中反應,亞鐵離子被過氧化氫氧化為三價鐵,過氧化氫被還原為水,離子方程式:2Fe2++H2O2+2H+═2Fe3++2H2O,
故答案為:2Fe2++H2O2+2H+═2Fe3++2H2O;
(4)E中有銨根離子,可取少量E于試管中,用膠頭滴管加入溶液,加熱試管,可觀察到試管口處濕潤的紅色石蕊試紙變藍,說明有銨根離子,
故答案為:取少量E于試管中,用膠頭滴管加入溶液,加熱試管,可觀察到試管口處濕潤的紅色石蕊試紙變藍;
(5)在C(FeSO4)溶液中加入氫氧化鈉和氧氣可以得到氫氧化鐵沉淀,反應的離子方程式為:2H2O+4Fe2++8OH-+O2═4Fe(OH)3↓,
故答案為:2H2O+4Fe2++8OH-+O2═4Fe(OH)3↓.
點評 本題考查了無機物質的推斷,物質轉化關系的突破推斷,主要考查鐵及其化合物的性質應用,氧化還原反應的判斷和書寫離子方程式,關鍵是濃硫酸和硫化亞鐵反應的離子方程式的書寫,題目難度較大.


科目:高中化學 來源: 題型:選擇題
| A. | 膠體的丁達爾效應與微粒直徑大小有關 | |
| B. | 電解質溶液的導電能力與溶液中離子濃度及離子所帶電荷多少有關 | |
| C. | CaO的水溶液能夠導電,因此Ca0是電解質 | |
| D. | 向飽和氯化鈉溶液中加人一小塊鈉,溶液中有固體析出 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該反應說明鈉是強還原劑,可用于冶煉金屬 | |
| B. | 該反應條件是TiCl4在熔融狀態或水溶液中 | |
| C. | Ti是氧化產物 | |
| D. | TiCl4是還原劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 三種元素在自然界中都只以化合態存在 | |
| B. | 三種元素的單質在化學反應中都只作氧化劑 | |
| C. | 實驗室可用NaOH溶液處理NO2和HCl廢氣 | |
| D. | 三種元素的氫化物(CH4、NH3、H2S)都易溶于水 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 銀是負極,銀片上有氣泡產生 | B. | 鋅片質量逐漸減少,銀片質量不變 | ||
| C. | 電流從鋅片經導線流向銀片 | D. | 氫離子在鋅片上被還原 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 羥基的電子式: | B. | 溴乙烷的電子式: | ||
| C. | 乙醇的結構簡式:CH3CH2OH | D. | CH4分子的球棍模型: |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com