
| A. | 0.1Lmol.L-1的硫酸銨溶液中:c(NH4+)+c(H+)>c(SO42-)+c(OH-) | |
| B. | 醋酸與醋酸鈉的pH=7的混合溶液中:c(CH3COO-)+c(CH3COOH)<c(Na+) | |
| C. | 將pH=5的H2SO4溶液稀釋1×103倍后,c(H+):c(SO42-)=2:1 | |
| D. | 常溫下,pH=4的NaHC2O4溶液中:c(C2O42-)<c(H2C2O4) |
分析 A.根據硫酸銨溶液中的電荷守恒判斷;
B.溶液為中性,則c(H+)=c(OH-),根據電荷守恒可知c(CH3COO-)=c(Na+),則c(CH3COO-)+c(CH3COOH)>c(Na+);
C.pH=5的H2SO4溶液中氫離子濃度為10-5mol/L,則硫酸根離子濃度為5×10-6mol/L,硫酸溶液稀釋后溶液仍然為酸性,氫離子濃度只能接近10-7mol/L;
D.常溫下,pH=4的NaHC2O4溶液中,HC2O4-的電離程度大于其水解程度.
解答 解:A.0.1Lmol.L-1的硫酸銨溶液中,根據電荷守恒可知:c(NH4+)+c(H+)=2c(SO42-)+c(OH-),則c(NH4+)+c(H+)>c(SO42-)+c(OH-),故A正確;
B.醋酸與醋酸鈉的pH=7的混合溶液中:則c(H+)=c(OH-),根據電荷守恒可知c(CH3COO-)=c(Na+),則c(CH3COO-)+c(CH3COOH)>c(Na+),故B錯誤;
C.pH=5的H2SO4溶液中氫離子濃度為10-5mol/L,則硫酸根離子濃度為5×10-6mol/L,稀釋過程中硫酸的物質的量不變,則稀釋后硫酸根離子的濃度為5×10-9mol/L;
硫酸溶液稀釋后溶液仍然為酸性,氫離子濃度只能接近10-7mol/L,所以稀釋后c(H+):c(SO42-)=10-7mol/L:5×10-9mol/L=20:1,故C錯誤;
D.常溫下,NaHC2O4溶液的pH=4,說明HC2O4-的電離程度大于其水解程度,則c(C2O42-)>c(H2C2O4),故D錯誤;
故選A.
點評 本題考查了離子濃度大小比較,題目難度中等,明確電荷守恒、物料守恒及鹽的水解原理為解答關鍵,C為易錯點,注意硫酸溶液稀釋后不可能變為堿性溶液.


科目:高中化學 來源: 題型:解答題


查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 活潑的金屬粉塵遇明火均易引起爆炸 | |
| B. | 任何金屬粉末在不正確操作下均可能引起爆炸 | |
| C. | 汽車輪轂表面鍍鋁既增加美觀度,又耐腐蝕 | |
| D. | 事故告誡人們安全生產,防污、防爆非常重要 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③ | B. | ②③④ | C. | ③⑤ | D. | ①③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cu2S在反應中既是氧化劑又是還原劑 | |
| B. | 以上反應中轉移電子的物質的量為1 mol | |
| C. | 以上參加反應的HNO3中被還原的HNO3為2 mol | |
| D. | 反應中,氧化劑和還原劑的物質的量之比為4:3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
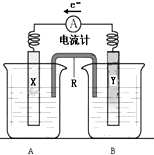 如圖是銅鋅原電池裝置.其電池的總反應是:
如圖是銅鋅原電池裝置.其電池的總反應是:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某學生在實驗室測定一未知濃度的稀鹽酸,已知25℃時,在20ml氫氧化鈉標準溶液中逐滴加入0.2mol/L醋酸溶液的PH變化曲線如圖所示:
某學生在實驗室測定一未知濃度的稀鹽酸,已知25℃時,在20ml氫氧化鈉標準溶液中逐滴加入0.2mol/L醋酸溶液的PH變化曲線如圖所示:| 實驗次數 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液體積 | 19.00 | 21.81 | 21.79 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com