

分析 (1)B為氧化爐,在氧化爐中氨氣與氧氣催化氧化生成一氧化氮和水;
(2)通入足量的氧氣,可以確保NO完全轉化成硝酸;
(3)①根據化合價升降相等配平該反應的方程式;
②據反應化學方程式反應物和生成物的性質和經濟效益分析,綠色化學為無污染,原子利用率高;
(4)根據NH3制NO的產率是96%、NO制HNO3的產率是92%,利用氮原子守恒來計算硝酸的量,再由HNO3跟NH3反應生成NH4NO3來計算氨氣的量,最后計算制HNO3所用去的NH3的質量占總耗NH3質量的百分數.
解答 解:(1)在上述工業制硝酸的生產中,B設備是進行氨的催化氧化反應,在氧化爐中進行;發生反應的方程式為:4NH3+5O2$\frac{\underline{\;催化劑\;}}{△}$4NO+6H2O,
故答案為:氧化爐;4NH3+5O2$\frac{\underline{\;催化劑\;}}{△}$4NO+6H2O;
(2)在合成硝酸的吸收塔中通入足量空,確保有充足的氧氣可使NO循環利用,全部轉化成HNO3,
故答案為:可使NO循環利用,全部轉化成HNO3;
(3)①氨氣分子中N元素的化合價為-3價,二氧化氮中N元素的化合價為+4價,氮氣中N元素化合價為0價,氨氣生成氮氣,化合價升高3價,二氧化氮生成氮氣,化合價降低4價,則化合價變化的最小公倍數為12,則氨氣的系數4,二氧化氮的系數為3,由于氮氣為雙原子分子,則氨氣的系數應該為8,二氧化氮的系數為6,然后根據質量守恒定律配平,配平后的反應為:8NH3+6NO2$\frac{\underline{\;催化劑\;}}{\;}$7N2+12H2O,
故答案為:8;6;7;12;
②綠色化學是要求反應對環境無污染、原子利用率高等優點,所以NH3還原法符合綠色化學,
故答案為:NH3還原法;
(4)根據氮原子守恒可知,NH3~NO~HNO3,
則1mol氨氣可得到硝酸的物質的量為:1mol×96%×92%=0.8832mol,
根據HNO3+NH3═NH4NO3可知反應消耗的氨氣的物質的量為:0.8832mol,
氨氣的質量之比等于物質的量之比,
則制HNO3所用去的NH3的質量占總耗NH3質量的百分數為:$\frac{1mol}{1mol+0.8832mol}$×100%≈53.1%,
故答案為:53.1.
點評 本題考查了工業制備原理應用、流程分析、實驗制備物質的分析判斷及利用物質的轉化及質量守恒的方法來進行簡單計算,題目難度中等,明確關系式法在化學計算中的應用,注意掌握工業制取硝酸的反應原理.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 0.1 mol•L-1Ba(OH)2溶液中含有0.2nA個OH- | |
| B. | 1mol Na與足量水反應,轉移2nA個電子 | |
| C. | 常溫常壓下,22.4L乙烯含有nA個CH2=CH2分子 | |
| D. | 常溫常壓下,46g NO2含有2nA個氧原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 序號 | 堆積方式 | 晶胞棱長(cm) |
| Ⅰ | 面心立方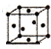 | a |
| Ⅱ | 體心立方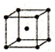 | b |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Q1>Q2 | |
| B. | 生成物總能量均高于反應物總能量 | |
| C. | 生成1mol HCl(g)放出Q1熱量 | |
| D. | 等物質的量時,Br2(g)具有的能量低于Br2(l) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 取浸取液少許,滴入AgNO3溶液有白色沉淀產生,則可能含有Cl- | |
| B. | 取浸取液少許,加入Cu和濃H2SO4,試管口有紅棕色氣體產生,則可能含有NO3- | |
| C. | 取浸取液少許,滴入硝酸酸化的BaCl2溶液,有白色沉淀產生,則一定含SO42- | |
| D. | 用潔凈的鉑絲棒蘸取浸取液,在酒精燈外焰上灼燒,焰色呈黃色,則一定含有Na+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| T/℃ | 30 | 40 | 50 |
| NH3的平衡濃度/(×10-6mol/L) | 4.8 | 5.9 | 6.0 |
| A. | 該反應的△H>0 | |
| B. | 常溫下該反應的△S>0 | |
| C. | 反應在30℃、40℃時化學平衡常數分別為K1、K2,則K1<K2 | |
| D. | 在常溫常壓下,人工固氮比較容易進行 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 最外層電子數:Z>R>Y | |
| B. | 氣態氫化物的穩定性:Y>Z | |
| C. | R、X的氧化物均為離子化合物 | |
| D. | X和Y兩者最高價氧化物對應的水化物能相互反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NO對環境的危害在于破壞臭氧層、形成酸雨等方面 | |
| B. | NO可以是某些高價N物質的還原產物也可以是某些含低價N物質的氧化產物 | |
| C. | 實驗室制取的NO可以用用排水法和向上排空氣法收集 | |
| D. | 生物體內存在少量NO能提高其生理機能,如擴張血管、促進免疫力 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com