
分析 ①碳酸氫鈉的化學式是NaHCO3,碳酸氫鈉俗稱不蘇打;
②因NaHCO3與HCl反應的化學方程式為:NaHCO3+HCl=NaCl+H2O+CO2↑,由此分書寫離子方程式;而胃潰瘍患者則不能服用它來治療胃酸過多,可用Al(OH)3代替;
③根據雜質碳酸氫鈉不穩定性除去.
解答 解:①碳酸氫鈉的化學式是NaHCO3,碳酸氫鈉俗稱不蘇打,故答案為:NaHCO3,小蘇打;
②因NaHCO3與HCl反應的化學方程式為:NaHCO3+HCl=NaCl+H2O+CO2↑,則反應的離子方程式為HCO3-+H+=H2O+CO2↑,而胃潰瘍患者則不能服用它來治療胃酸過多,可用Al(OH)3代替,故答案為:HCO3-+H+=H2O+CO2↑;Al(OH)3;
③除去碳酸鈉固體中碳酸氫鈉的方法為加熱,方程式為:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,故答案為:加熱;2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
點評 本題綜合考查了Na2CO3和NaHCO3的性質,側重于學生的分析能力和元素化合物知識的綜合運用的考查,試題內容簡單,只要掌握基礎知識就可完成.


 智慧小復習系列答案
智慧小復習系列答案科目:高中化學 來源: 題型:解答題
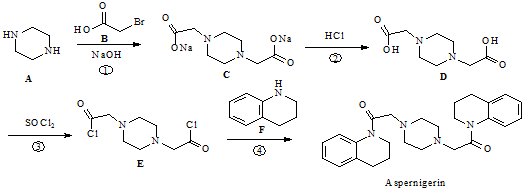
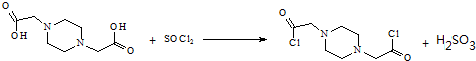 .
.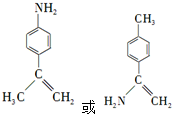 .
.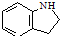 為原料,利用上述有關信息,寫出制備
為原料,利用上述有關信息,寫出制備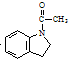 的合成路線流程圖(無機試劑任用).合成路線流程圖例如下:CH2═CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH
的合成路線流程圖(無機試劑任用).合成路線流程圖例如下:CH2═CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙醛和乙酸乙酯 | B. | 甲酸和乙酸 | ||
| C. | 甲醛和乙醇 | D. | 甲酸甲酯和乙酸乙酯 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
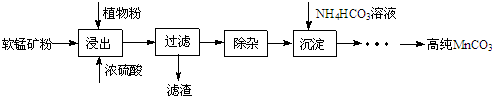
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| T/K | 298 | 398 | 498 |
| 平衡常數K | 4.1×106 | K1 | K2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 作為測量中和反應反應熱的裝置圖,從玻璃儀器的角度看,圖1還缺少環形玻璃攪拌棒 | |
| B. | 檢驗圖2裝置的氣密性時,向漏斗中加水若出現圖中所示的現象,可以證明該氣密性良好 | |
| C. | 已知圖3是利用原電池檢驗空氣中Cl2含量的裝置,其中Pt電極作負極 | |
| D. | 根據圖4的溶解度變化可知,在較低溫度下容易分離MgSO4•7H2O和CaSO4•2H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com