

| 物質 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| 溶解度(g/100g水) | 0℃ | 28 | 35.7 | 4.7 | 163 |
| 40℃ | 40.1 | 36.4 | 26.3 | 215 | |
| 80℃ | 51.3 | 38 | 73 | 376 | |
分析 鉻鐵礦通過焙燒,得到Na2CrO4、Fe2O3、MgO和NaAlO2的混合體系,然后加水溶解,過濾分離,得到固體Fe2O3、MgO,濾液中含有Na2CrO4、NaAlO2,再調節溶液的pH,使偏鋁酸鹽完全轉化為氫氧化鋁沉淀,過濾分離,濾液繼續調節pH使CrO42-轉化為Cr2O72-,最后向所得溶液中加入氯化鉀,利用溶解度不同,從溶液中析出溶解度更小的K2Cr2O7晶體.
(1)操作I是將互不相溶的固體與液態分離,由上述分析可知,固體X含有氧化鐵、氧化鎂;
(2)用醋酸調節溶液pH=7~8,使偏鋁酸鹽完全轉化為氫氧化鋁沉淀,再進行過濾分離而除去;
(3)Cr2O72-具有強氧化性,將氯離子氧化為氯氣,還原得到Cr3+;
(4)由表中溶解度數據,可知四種物質中K2Cr2O7的溶解度最小,符合復分解反應條件;
(5)①由電荷守恒可知,缺項物質為H+,產物中n[Fe(OH)3]:n(H2)=1:1,設二者系數均為1,根據電子轉移守恒,計算Cr(OH)3的系數,再利用電荷守恒、原子守恒配平,然后擴大倍數配平后離子方程式;
②鉻含量最高限值是0.052mg/L,則溶液中c(Cr3+)=1×10-6mol/L,將c(Cr3+)代入Ksp=c(Cr3+)×c3(OH-)計算溶液中c(OH-)的極小值,進而計算溶液pH最小值.
解答 解:鉻鐵礦通過焙燒,得到Na2CrO4、Fe2O3、MgO和NaAlO2的混合體系,然后加水溶解,過濾分離,得到固體Fe2O3、MgO,濾液中含有Na2CrO4、NaAlO2,再調節溶液的pH,使偏鋁酸鹽完全轉化為氫氧化鋁沉淀,過濾分離,濾液繼續調節pH使CrO42-轉化為Cr2O72-,最后向所得溶液中加入氯化鉀,利用溶解度不同,從溶液中析出溶解度更小的K2Cr2O7晶體.
(1)操作I是將互不相溶的固體與液態分離,采取過濾方法分離,由上述分析可知,固體X含有Fe2O3、MgO,
故答案為:過濾;Fe2O3、MgO;
(2)用醋酸調節溶液pH=7~8,使偏鋁酸鹽完全轉化為氫氧化鋁沉淀,再進行過濾分離而除去,操作Ⅱ所得固體Y的成分為Al(OH)3,
故答案為:Al(OH)3;
(3)Cr2O72-具有強氧化性,將氯離子氧化為氯氣,還原得到Cr3+,反應離子方程式為:Cr2O72-+6Cl-+14H+=2 Cr3++3Cl2↑+7 H2O,
故答案為:Cr2O72-+6Cl-+14H+=2 Cr3++3Cl2↑+7 H2O;
(4)由表中溶解度數據,可知K2Cr2O7的溶解度比Na2Cr2O7小(或四種物質中K2Cr2O7的溶解度最小),符合復分解反應條件,故反應可以發生,
故答案為:K2Cr2O7的溶解度比Na2Cr2O7小(或四種物質中K2Cr2O7的溶解度最小);
(5)①由電荷守恒可知,缺項物質為H+,產物中n[Fe(OH)3]:n(H2)=1:1,設二者系數均為1,根據電子轉移守恒,Cr(OH)3的系數為$\frac{1×3-1×2}{6-3}$=$\frac{1}{3}$,再利用電荷守恒、原子守恒、擴大倍數配平后離子方程式為:6Fe+Cr2O72-+2H++17H2O=6Fe(OH)3↓+2Cr(OH)3↓+6H2↑,
故答案為:6,1,2H+,17,6,2,6;
②鉻含量最高限值是0.052mg/L,則溶液中c(Cr3+)=1×10-6mol/L,由代入Ksp=c(Cr3+)×c3(OH-),可知溶液中c(OH-)的極小值為$\root{3}{\frac{6.4×1{0}^{-32}}{1×1{0}^{-6}}}$mol/L=4×10-9mol/L,溶液pH最小值=-lg$\frac{1{0}^{-14}}{4×1{0}^{-9}}$=5.6,
故答案為:5.6.
點評 本題考查化學實驗制備方案,涉及對原理的分析評價、物質的分離提純、氧化還原反應配平、溶度積有關計算等,需要學生具備扎實的基礎,理解工藝流程原理是解題關鍵,難度中等.


 互動課堂系列答案
互動課堂系列答案 激活思維智能訓練課時導學練系列答案
激活思維智能訓練課時導學練系列答案科目:高中化學 來源: 題型:選擇題
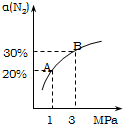 某溫度下,對于反應N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol.N2的平衡轉化率(α)與體系總壓強(P)的關系如圖所示.下列說法正確的是( )
某溫度下,對于反應N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol.N2的平衡轉化率(α)與體系總壓強(P)的關系如圖所示.下列說法正確的是( )| A. | 將1.0mol氮氣、3.0mol氫氣,置于1L密閉容器中發生反應,放出的熱量為92.4kJ | |
| B. | 平衡狀態由A變到B時,平衡常數K(A)<K(B) | |
| C. | 上述反應在達到平衡后,增大壓強,H2的轉化率提高 | |
| D. | 保持壓強不變,通入惰性氣體,平衡常數不變,平衡不移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

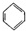 +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$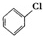 +HCl
+HCl| 項目 | 二氯苯 | 尾氣 | 不確定苯耗 | 流失總量 |
| 苯流失量(kg/t) | 13 | 24.9 | 51.3 | 89.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放出1780kJ的能量 | B. | 放出1220kJ的能量 | ||
| C. | 放出450kJ的能量 | D. | 吸收430kJ的能量 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
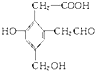 ,取足量的Na、NaOH和新制Cu(OH)2分別與等物質的量的A在一定條件下充分反應時,理論上需 Na、NaOH和新制Cu(OH)2三種物質的物質的量之比為3:2:3.
,取足量的Na、NaOH和新制Cu(OH)2分別與等物質的量的A在一定條件下充分反應時,理論上需 Na、NaOH和新制Cu(OH)2三種物質的物質的量之比為3:2:3.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 .
. ;D、E形成的化合物:
;D、E形成的化合物: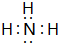 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com