
| 2mol |
| 2.5mol×22.4L/mol |


科目:高中化學 來源: 題型:
| A、石油分餾時分子中碳原子數較少的烴先汽化 |
| B、石油分餾得到的汽油是純凈物 |
| C、石油的分餾和煤的干餾都是化學變化 |
| D、將煤直接加強熱使其分解,叫做煤的干餾 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 科學研究表明,月球上可能存在少量水:月巖中含有鈦鐵礦,其主要成分的晶胞如圖所示.
科學研究表明,月球上可能存在少量水:月巖中含有鈦鐵礦,其主要成分的晶胞如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:
| 3 |
| 4 |
查看答案和解析>>
科目:高中化學 來源: 題型:
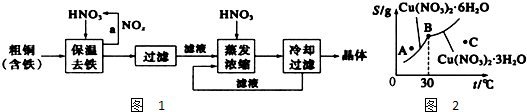
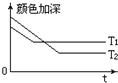 (1)反應A+B?2C,其中A為有色氣態物質,其混合物顏色深淺與反應時間,溫度(T)之間的關系如圖所示(B、C均為無色物質):
(1)反應A+B?2C,其中A為有色氣態物質,其混合物顏色深淺與反應時間,溫度(T)之間的關系如圖所示(B、C均為無色物質):查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
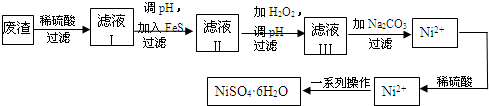
 鈰、鉻、鈷、鎳雖不是中學階段常見的金屬元素,但在工業生產中有著重要作用.
鈰、鉻、鈷、鎳雖不是中學階段常見的金屬元素,但在工業生產中有著重要作用.| 放電 |
| 充電 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、不需要通過化學反應就能從海水中獲得食鹽和淡水 |
| B、鐵在潮濕的空氣中放置,易發生化學腐蝕而生銹 |
| C、高空臭氧層吸收太陽紫外線,保護地球生物;低空過量臭氧是污染氣體,對人體有害 |
| D、氯氣與燒堿溶液或石灰乳反應都能得到含氯消毒劑 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com