
 硫酰氯(SO2Cl2)常作氯化劑或氯磺化劑,用于制作藥品、染料、表面活性劑等.有關物質的部分性質如表:
硫酰氯(SO2Cl2)常作氯化劑或氯磺化劑,用于制作藥品、染料、表面活性劑等.有關物質的部分性質如表:| 物質 | 熔點/℃ | 沸點/℃ | 其它性質 |
| SO2Cl2 | -54.1 | 69.1 | ①易水解,產生大量白霧 ②易分解:SO2Cl2$\frac{\underline{\;100℃\;}}{\;}$SO2↑+Cl2↑ |
| H2SO4 | 10.4 | 338 | 吸水性且不易分解 |
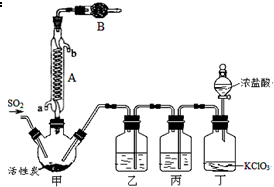
分析 二氧化硫和氯氣合成硫酰氯:甲裝置:SO2(g)+Cl2(g)$\frac{\underline{\;活性炭\;}}{\;}$SO2Cl2;硫酰氯會水解,儀器B中盛放的藥品是堿石灰防止空氣中的水蒸氣進入裝置,同時吸收揮發出去的二氧化硫和氯氣,丁裝置:濃鹽酸和氯酸鉀反應制取氯氣,濃鹽酸易揮發,制取的氯氣中含有氯化氫,丙裝置:除去Cl2中的HCl,乙裝置:干燥氯氣.
(1)根據采用逆流的冷凝效果好,判斷冷凝管的進水口;
(2)儀器B中盛放的藥品是堿石灰防止空氣中的水蒸氣進入裝置,同時吸收揮發出去的二氧化硫和氯氣;
(3)實驗時,裝置丁中氯酸鉀+5價的氯和鹽酸中-1價的氯發生氧化還原反應生成氯氣;
(4)鹽酸易揮發,制取的氯氣中含有氯化氫,丙裝置:除去Cl2中的HCl;SO2Cl2遇水生成硫酸和氯化氫,根據原子守恒書寫;
(5)①二者沸點相差較大,采取蒸餾法進行分離;
②氯磺酸(ClSO3H)分解:2ClSO3H═H2SO4+SO2Cl2,設計實驗方案檢驗產品,需檢驗氫離子、檢驗硫酸根離子.
解答 解:(1)根據采用逆流的冷凝效果好,所以冷凝管中的冷卻水進口為a,
故答案為:a;
(2)甲裝置:SO2(g)+Cl2(g)$\frac{\underline{\;活性炭\;}}{\;}$SO2Cl2,二氧化硫、氯氣為有毒的酸性氣體,產物硫酰氯會水解,所以儀器B中盛放的藥品是堿性物質堿石灰,可防止空氣中的水蒸氣進入裝置,同時吸收揮發出去的二氧化硫和氯氣,
故答案為:堿石灰;
(3)濃鹽酸和氯酸鉀發生反應生成KCl、氯氣和水,反應為:6HCl(濃)+KClO3=KCl+3Cl2↑+3H2O,離子方程式為:ClO3-+5Cl-+6H+=3Cl2↑+3H2O,
故答案為:ClO3-+5Cl-+6H+=3Cl2↑+3H2O;
(4)鹽酸易揮發,制取的氯氣中含有氯化氫,氯氣難溶于飽和食鹽水;HCl易溶于水,而氯氣難溶于飽和食鹽水,可用飽和NaCl溶液除去Cl2中的少量HCl,所以丙裝置作用為誒:除去Cl2中的HCl,SO2Cl2遇水生成硫酸和氯化氫,則其水解方程式為:SO2Cl2+2H2O═H2SO4+2HCl,
故答案為:除去Cl2中的HCl;SO2Cl2+2H2O═H2SO4+2HCl;
(5)①二者為互溶液體,沸點相差較大,采取蒸餾法進行分離,
故答案為:蒸餾;
②氯磺酸(ClSO3H)分解:2ClSO3H$\frac{\underline{\;\;△\;\;}}{\;}$H2SO4+SO2Cl2,取產物在干燥條件下加熱至完全反應(或揮發或分解等),冷卻后加水稀釋;取少量溶液滴加紫色石蕊試液變紅,證明溶液呈酸性,再取少量溶液,加入BaCl2溶液產生白色沉淀,說明含有H2SO4,或取反應后的產物直接加BCl2溶液,有白色沉淀,證明含有硫酸根離子,再滴加紫色石蕊試液變紅,說明含有H2SO4,
故答案為:取產物在干燥條件下加熱至完全反應(或揮發或分解等),冷卻后加水稀釋;取少量溶液滴加紫色石蕊試液變紅;再取少量溶液,加入BaCl2溶液產生白色沉淀,說明含有H2SO4.或取反應后的產物直接加BCl2溶液,有白色沉淀,再滴加紫色石蕊試液變紅,說明含有H2SO4.
點評 本題考查實驗制備方案,涉及對反應原理、裝置及操作的分析評價、對儀器的識別、物質的分離提純等,注意對物質性質信息的應用,難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋅 | B. | 鐵 | C. | 鎂 | D. | 鋁 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
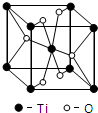 第四周期過渡元素Mn、Fe、Ti可與C、H、O形成多種化合物.
第四周期過渡元素Mn、Fe、Ti可與C、H、O形成多種化合物.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
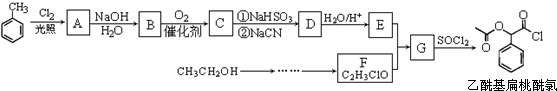
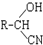 ,RCN$\stackrel{H_{2}O/H+}{→}$RCOOH,RCOOH$\stackrel{SOCl_{2}}{→}$RCOCl$\stackrel{R′OH}{→}$RCOOR′
,RCN$\stackrel{H_{2}O/H+}{→}$RCOOH,RCOOH$\stackrel{SOCl_{2}}{→}$RCOCl$\stackrel{R′OH}{→}$RCOOR′ ,E中含氧官能團的名稱醇羥基和羧基.
,E中含氧官能團的名稱醇羥基和羧基.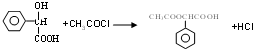 .
.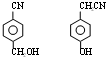 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④②⑤③ | B. | ④①②⑤③ | C. | ②④⑤①③ | D. | ⑤②④①③ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com