
【題目】化合物G是合成抗心律失常藥物決奈達隆的一種中間體,可通過以下方法合成: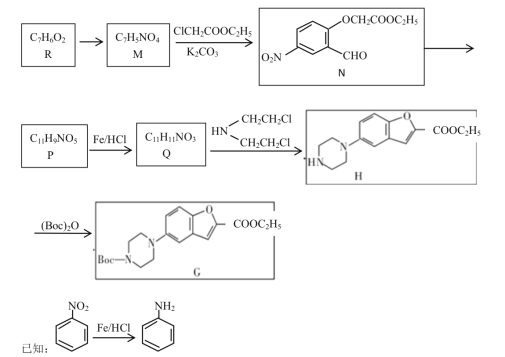
請回答下列問題:
(1)R的名稱是_______________;N中含有的官能團數目是______。
(2)M→N反應過程中K2CO3的作用是____________________________________。
(3)H→G的反應類型是______________。
(4)H的分子式________________。
(5)寫出Q→H的化學方程式:___________________________________。
(6)T與R組成元素種類相同,符合下列條件T的同分異構體有_____種。
①與R具有相同官能團;②分子中含有苯環;③T的相對分子質量比R多14
其中在核磁共振氫譜上有5組峰且峰的面積比為1:1:2:2:2的結構簡式有___________。
(7)以1,5-戊二醇(![]() ) 和苯為原料(其他無機試劑自選)合成
) 和苯為原料(其他無機試劑自選)合成![]() ,設計合成路線:_________________________________________。
,設計合成路線:_________________________________________。
【答案】鄰羥基苯甲醛(或2-羥基苯甲醛) 4 消耗產生的HCl,提高有機物N的產率 取代反應 C15H18N2O3 ![]() +
+![]() →2HCl+
→2HCl+ 17
17  、
、

【解析】
R在一定條件下反應生成M,M在碳酸鉀作用下,與ClCH2COOC2H5反應生成N,根據N的結構簡式,M的結構簡式為 ,根據R和M的分子式,R在濃硫酸、濃硝酸作用下發生取代反應生成M,則R的結構簡式為
,根據R和M的分子式,R在濃硫酸、濃硝酸作用下發生取代反應生成M,則R的結構簡式為 ,N在一定條件下反應生成P,P在Fe/HCl作用下生成Q,Q與
,N在一定條件下反應生成P,P在Fe/HCl作用下生成Q,Q與![]() 反應生成H,根據H的結構簡式和已知信息,則Q的結構簡式為
反應生成H,根據H的結構簡式和已知信息,則Q的結構簡式為![]() ,P的結構簡式為:
,P的結構簡式為: ;H在(Boc)2O作用下反應生成G,據此分析解答。
;H在(Boc)2O作用下反應生成G,據此分析解答。
(1)根據分析, R的結構簡式為 ,名稱是鄰羥基苯甲醛(或2-羥基苯甲醛);根據N的結構簡式,其中含有的官能團有醚基、酯基、硝基、醛基,共4種官能團;
,名稱是鄰羥基苯甲醛(或2-羥基苯甲醛);根據N的結構簡式,其中含有的官能團有醚基、酯基、硝基、醛基,共4種官能團;
(2)M在碳酸鉀作用下,與ClCH2COOC2H5反應生成N,根據N的結構簡式,M的結構簡式為 ,根據結構變化,M到N發生取代反應生成N的同時還生成HCl,加入K2CO3可消耗產生的HCl,提高有機物N的產率;
,根據結構變化,M到N發生取代反應生成N的同時還生成HCl,加入K2CO3可消耗產生的HCl,提高有機物N的產率;
(3)Q與![]() 反應生成H,Q的結構簡式為
反應生成H,Q的結構簡式為![]() ,Q中氨基上的氫原子被取代,H→G的反應類型是取代反應;
,Q中氨基上的氫原子被取代,H→G的反應類型是取代反應;
(4)結構式中,未標注元素符號的每個節點為碳原子,每個碳原子連接4個鍵,不足鍵由氫原子補齊,H的分子式C15H18N2O3;
(5)Q與![]() 反應生成H,Q的結構簡式為
反應生成H,Q的結構簡式為![]() ,Q→H的化學方程式:
,Q→H的化學方程式:![]() +
+![]() →2HCl+
→2HCl+ ;
;
(6) R的結構簡式為 ,T與R組成元素種類相同,①與R具有相同官能團,說明T的結構中含有羥基和醛基;②分子中含有苯環;③T的相對分子質量比R多14,即T比R中多一個-CH2-,若T是由
,T與R組成元素種類相同,①與R具有相同官能團,說明T的結構中含有羥基和醛基;②分子中含有苯環;③T的相對分子質量比R多14,即T比R中多一個-CH2-,若T是由 和-CH3構成,則連接方式為
和-CH3構成,則連接方式為 ;若T是由
;若T是由 和-CH3構成,則連接方式為
和-CH3構成,則連接方式為 ;若T是由
;若T是由 和-CH3構成,則連接方式為
和-CH3構成,則連接方式為 ;若T是由
;若T是由 和-CHO構成,則連接方式為
和-CHO構成,則連接方式為 ;若T是由
;若T是由 和-OH構成,則連接方式為
和-OH構成,則連接方式為 ;若T是由
;若T是由![]() 和-CH(OH)CHO構成,則連接方式為
和-CH(OH)CHO構成,則連接方式為![]() ,符合下列條件T的同分異構體有17種;其中在核磁共振氫譜上有5組峰且峰的面積比為1:1:2:2:2,說明分子中含有5種不同環境的氫原子,結構簡式有
,符合下列條件T的同分異構體有17種;其中在核磁共振氫譜上有5組峰且峰的面積比為1:1:2:2:2,說明分子中含有5種不同環境的氫原子,結構簡式有 、
、 ;
;
(7)以1,5-戊二醇(![]() ) 和苯為原料,依據流程圖中Q→F的信息,需將以1,5-戊二醇轉化為1,5-二氯戊烷,將本轉化為硝基苯,再將硝基苯轉化為苯胺,以便于合成目標有機物
) 和苯為原料,依據流程圖中Q→F的信息,需將以1,5-戊二醇轉化為1,5-二氯戊烷,將本轉化為硝基苯,再將硝基苯轉化為苯胺,以便于合成目標有機物![]() ,設計合成路線:
,設計合成路線: 。
。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】汽車尾氣中NO產生的反應為:N2(g)+O2(g)![]() 2NO(g),一定條件下,等物質的量的N2(g)和O2(g)在恒容密閉容器中反應,下圖曲線a表示該反應在溫度T下N2的濃度隨時間的變化,曲線b表示該反應在某一起始反應條件改變時N2的濃度隨時間的變化。下列敘述正確的是:
2NO(g),一定條件下,等物質的量的N2(g)和O2(g)在恒容密閉容器中反應,下圖曲線a表示該反應在溫度T下N2的濃度隨時間的變化,曲線b表示該反應在某一起始反應條件改變時N2的濃度隨時間的變化。下列敘述正確的是:

A. 溫度T下,該反應的平衡常數K=![]()
B. 溫度T下,隨著反應的進行,混合氣體的密度減小
C. 曲線b對應的條件改變可能是加入了催化劑
D. 若曲線b對應的條件改變是溫度,可判斷該反應的△H<0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鏈狀有機物A是一種食用型香精,在一定條件下有如下變化:
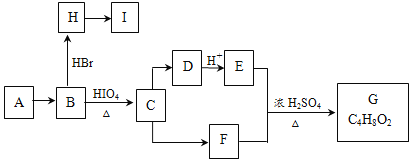
已知:(1)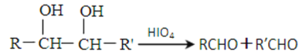
(2)A和G互為同分異構體,A不能使Br2的CCl4溶液褪色。B和F中所含官能團的類型相同。
完成下列填空:
(1)F的分子式為________________;C→D的反應類型是__________________________。
(2)A的結構簡式為________________________________。
(3)若C中混有少量的E,請寫出相應的除雜試劑和分離方法:________________。
(4)I中所有碳原子均在一條直線上,H轉化為I的化學方程式為:______________________。
(5)X是A的一種同分異構體,1mol X在HIO4加熱條件下完全反應,可以生成1mol無支鏈有機物,則X的結構簡式為_________________。
(6)設計有1-丁烯為原料,合成H的合成路線。(合成路線常用的表示方式為:甲![]() 乙……
乙……![]() 目標產物)______________________________________
目標產物)______________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】FeCl3是中學實驗室常用的試劑。
(1)寫出氯化鐵在水中的電離方程式:_________。
(2)利用氯化鐵溶液制備氫氧化鐵膠體。
①下列制備氫氧化鐵膠體的操作方法正確的是_______(填字母)。
A.向飽和氯化鐵溶液中滴加適量的氫氧化鈉稀溶液
B.加熱煮沸氯化鐵飽和溶液
C.在氨水中滴加氯化鐵濃溶液
D.在沸水中滴加飽和氯化鐵溶液,煮沸至出現紅褐色液體
②區別氯化鐵溶液和氫氧化鐵膠體的方法是___________。
(3)為了探究離子反應的本質,設計如下實驗:
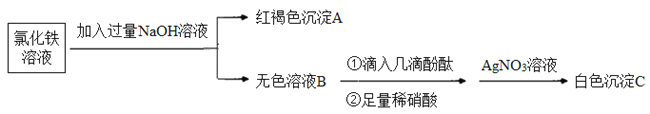
①寫出生成A的離子方程式:_________。
②上述流程中,加入足量稀硝酸的目的是________。如何判定無色溶液B與稀硝酸發生了離子反應?________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有以下幾種有機物:
①![]() ②
②![]() ③
③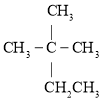 ④
④![]() ⑤
⑤![]()
⑥![]() ⑦
⑦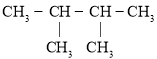 ⑧
⑧![]() ⑨
⑨![]()
請利用上述給出的物質按要求回答下列問題:
(1)③的系統命名是________。
(2)用“>”表示①③④⑧熔沸點高低順序:________(填序號)。
(3)與③互為同系物的是________(填序號)。
(4)⑨的一氯代物同分異構體數目有________種。
(5)在120℃,![]() 條件下,某種氣態烴與足量的
條件下,某種氣態烴與足量的![]() 完全反應后,測得反應前后氣體的體積沒有發生改變,則該烴是________(填序號)。
完全反應后,測得反應前后氣體的體積沒有發生改變,則該烴是________(填序號)。
(6)寫出⑥在鐵作催化劑的條件下與液溴發生取代反應的化學方程式________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作能達到實驗目的的是

A. 用經水濕潤的pH試紙測量溶液的pH
B. 將4.0 g NaOH固體置于100 mL容量瓶中,加水至刻度,配制1.000 mol·L1NaOH溶液
C. 用裝置甲蒸干AlCl3溶液制無水AlCl3固體
D. 用裝置乙除去實驗室所制乙烯中的少量SO2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設 NA為阿伏加德羅常數的值,下列說法正確的是( )
A.足量銅與 100mL 18mol/L 的濃硫酸在一定條件下反應轉移的電子數目為1.8 NA
B.常溫下,pH=13 的氫氧化鈉溶液中由水電離出的H+的數目為 10-13NA
C.標準狀況下,2.24 L CCl4含有的共價鍵數為 0.4NA
D.加熱條件下,16g O2、O3的混合氣體與足量鎂粉充分反應轉移的電子數目為 2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用圖所示裝置檢驗乙烯時不需要除雜的是

乙烯的制備 | 試劑X | 試劑Y | |
A | CH3CH2Br與NaOH乙醇溶液共熱 | H2O | KMnO4酸性溶液 |
B | CH3CH2Br與NaOH乙醇溶液共熱 | H2O | Br2的CCl4溶液 |
C | CH3CH2OH與濃H2SO4共熱至170℃ | NaOH溶液 | KMnO4酸性溶液 |
D | CH3CH2OH與濃H2SO4共熱至170℃ | NaOH溶液 | Br2的CCl4溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下,向某Na2CO3和NaHCO3的混合溶液中逐滴加入BaCl2溶液,溶液中lgc(Ba2+)與![]() 的變化關系如圖所示。下列說法正確的是( )
的變化關系如圖所示。下列說法正確的是( )
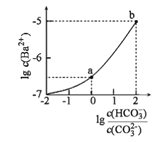
(已知:H2CO3的Ka1、Ka2分別為4.2×10-7、5.6×10-11)
A.a對應溶液的pH小于b
B.b對應溶液的c(H+)=4.2×10-7mol·L-1
C.a→b對應的溶液中![]() 減小
減小
D.a對應的溶液中一定存在:2c(Ba2+)+c(Na+)+c(H+)=3c(HCO3-)+c(Cl-)+c(OH-)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com