
X、Y、Z、M、N代表五種金屬,有以下化學反應:
(1)水溶液中:X+Y2+=X2++Y;
(2)Z+2 H2O(冷水)=Z(OH) 2+H2↑
(3)M、N 為電極,與N鹽溶液組成原電池,電極反應為:M-2e-=M2+
(4)Y 可以溶于稀硫酸中,M不被稀硫酸氧化。則這五種金屬的活潑性由弱到強的順序是
A.M<N<Y<X<Z B.N<M<X<Y<Z
C.N<M<Y<X<Z D.X<Z<N<M<Y
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源:2016-2017學年山西省高二12月月考化學試卷(解析版) 題型:選擇題
室溫下,下列溶液等體積混合后,所得溶液的pH一定大于7的是
A.0.1 mol/L的鹽酸和0.1 mol/L的氫氧化鈉溶液
B.0.1 mol/L的硫酸和0.1 mol/L的氫氧化鋇溶液
C.pH=4的醋酸溶液和pH=10的氫氧化鈉溶液
D.pH=4的醋酸溶液和pH=10的氨水溶液
查看答案和解析>>
科目:高中化學 來源:2016-2017學年內蒙古高一期中化學卷(解析版) 題型:選擇題
甲、乙、丙、丁分別是氫氧化鈣溶液、硝酸鉀溶液、碳酸鈉溶液、鹽酸中的一種。已知甲和丙可以反應,甲和丁也可以反應,則下列說法正確的是
 A.甲一定是氫氧化鈣溶液 B.乙一定是硝酸鉀溶液
A.甲一定是氫氧化鈣溶液 B.乙一定是硝酸鉀溶液
C.丙不可能是碳酸鈉溶液 D.丁只能是鹽酸
查看答案和解析>>
科目:高中化學 來源:2016-2017學年內蒙古高一期中化學卷(解析版) 題型:選擇題
氧化還原反應的實質是
A.分子中的原子重新組合 B.氧元素的得失
C.電子的得失或共用電子對的偏移 D.化合價的改變
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上段考二化學試卷(解析版) 題型:填空題
己知可逆反應AsO43-+2I-+2H+ AsO33-+I2+H2O,設計如下圖裝置,進行下述操作:
AsO33-+I2+H2O,設計如下圖裝置,進行下述操作:
①向(Ⅱ)燒杯中逐滴加入濃鹽酸,發現微安表(G)指針偏轉;②若改往(Ⅱ)燒杯中滴加40%NaOH溶液,發現微安表指針與①的偏轉方向相反。回答下列問題

(1)操作①過程中,C1棒為__________極,C2棒上發生的反應為______________________
(2)操作②過程中鹽橋中的_________離子移向(I)燒杯,C1棒上發生的反應為_____________
(3)若將微安表換成電解冶煉鋁裝置,寫出電解總反應方程式__________________________________
(4)若將微安表換成電解精煉銅裝置,在操作②過程中與C2棒連接的為_________電極,電解一段時間后,溶液中CuSO4溶液的濃度_____________(填“變大”“變小”或“不變”)
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上段考二化學試卷(解析版) 題型:選擇題
用0.1000mol·L-1NaOH溶液滴定未知濃度的鹽酸,選用酚酞為指示劑,造成測定結果偏高的原因可能是
A.盛裝待測液的錐形瓶用蒸餾水洗過,沒用待測液潤洗
B.酸式滴定管在使用前未用待測液鹽酸潤洗
C.滴定前堿式滴定管尖嘴中有氣泡,滴定后氣泡消失
D.滴定前讀數平視,滴定終點讀數時俯視堿式滴定管的刻度
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上段考二化學試卷(解析版) 題型:選擇題
電池是人類生產和生活的重要能量來源,各式各樣電池的發展是化學對人類的一項重大貢獻。下列有關電池的敘述正確的是
A.鋅錳干電池工作一段時間后碳棒變細
B.氫氧燃料電池可將熱能直接轉變為電能
C.在現實生活中,電化學腐蝕要比化學腐蝕嚴重的多,危害更大
D.太陽能電池的主要材料是高純度的二氧化硅
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省高二11月月考化學試卷(解析版) 題型:選擇題
己知NA是阿伏加徳羅常數,下列說法正確的是( )
A. 7.lg氯氣與足量的氫氧化鈉溶液反應轉移的電子數為0.2NA
B. V L amol/L的氯化鐵溶液中,若Fe3+的數目為NA,則Cl-的數目大于3NA
C. 標準狀況下,22.4LNO和11.2LO2混合后氣體的分子總數為1.0NA
D. 工業用電解法進行粗銅精煉時,毎轉移lmol電子,陽極上溶解的銅原子數必為0.5NA
查看答案和解析>>
科目:高中化學 來源:2017屆福建省高三上學期期中化學試卷(解析版) 題型:填空題
鈦、鉻、鐵、鎳、銅等金屬及其化合物在工業上有重要用途。
(1)鈦鐵合金是鈦系儲氫合金的代表,該合金具有放氫溫度低、價格適中等優點。
①Ti的基態原子價電子排布式為________________。
②Fe的基態原子共有________種不同能級的電子。
(2)制備CrO2Cl2的反應為K2Cr2O7+3CCl4===2KCl+2CrO2Cl2+3COCl2↑。
①上述化學方程式中非金屬元素電負性由大到小的順序是______________(用元素符號表示)。
②COCl2分子中所有原子均滿足 8電子構型,COCl2分子中σ鍵和π鍵的個數比為____________,中心原子的雜化方式為____________。
8電子構型,COCl2分子中σ鍵和π鍵的個數比為____________,中心原子的雜化方式為____________。
(3)NiO、FeO的晶體結構均與氯化鈉的晶體結構相同,其中Ni2+和Fe2+的離子半徑分別為6.9×10-2 nm和7.8×10-2 nm。則熔點:NiO____________(填“>”、“<”或“=”)FeO。
(4)Ni和La的合金是目前使用廣泛的儲氫材料,具有大容量、高壽命、耐低溫等特點,在日本和中國已實現了產業化。該合金的晶胞結構如圖所示。
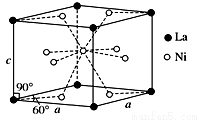
①該晶體的化學式為________________。
②已知該晶胞的摩爾質量為M g·mol-1,密度為d g·cm-3。設NA為阿伏加德羅常數的值,則該晶胞的體積是____________cm3(用含M、d、NA的代數式表示)。
[化學—選修5:有機化學基礎]
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com