
| A. | 放電時,負極的電極反應式:Li-e-═Li+ | |
| B. | 充電時,LiFePO4既發生氧化反應又發生還原反應 | |
| C. | 該電池不能用水溶液作為電解質 | |
| D. | 放電過程中Li+向負極移動 |
分析 根據鋰離子電池的電池反應式為:Li+FePO4 $?_{放電}^{充電}$ LiFePO4,可知,放電時,Li的化合價升高,被氧化,為原電池的負極,負極的電極反應式:Li-e-=Li+;充電時,反應逆向進行,反應物只有一種,故化合價既有升,又有降,所以既發生氧化反應又發生還原反應;由于Li可以與水反應,故應為非水材料;原電池工作時,陽離子向正極移動,陰離子向負極移動,據此分析.
解答 解:A.放電時,Li的化合價升高,被氧化,為原電池的負極,負極的電極反應式:Li-e-=Li+,故A正確;
B、充電時,LiFePO4的Fe的化合價升高,Fe元素被氧化,Li的化合價降低,Li元素被還原,所以LiFePO4既發生氧化反應又發生還原反應,故B正確;
C、Li很活潑,會與水反應,不能用水溶液,故C正確;
D、原電池中陽離子向正極移動,即Li+向正極移動,故D錯誤;
故選:D.
點評 本題考查電化學的熱點-鋰離子電池,根據總反應式判斷出正負極和陰陽極的反應,從化合價變化的角度分析,注意把握Li的化學性質,題目難度中等.


 名師點睛字詞句段篇系列答案
名師點睛字詞句段篇系列答案科目:高中化學 來源: 題型:選擇題
| 實 驗 方 案 | 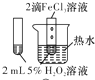 | 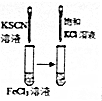 | 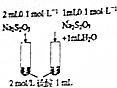 | 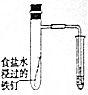 |
| 目 的 | A.驗證升高溫度可加快H2O2分解 | B.探究增大c(Cl-使平衡逆向移動 | C.探究濃度對化學反應速率的影響 | D.驗證鐵發生析氫腐蝕 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 蒸發、結晶 | B. | 過濾、分液 | C. | 過濾、蒸餾 | D. | 萃取、分液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 8種 | B. | 10種 | C. | 11種 | D. | 12種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 推廣使用太陽能、風能、海洋能、氫能,有利于緩解溫室效應 | |
| B. | 乙醇和汽油都是可再生能源,應大力推廣“乙醇汽油” | |
| C. | 用電解水的方法制取大量氫氣可以緩解能源不足的問題 | |
| D. | 升高溫度活化能降低 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
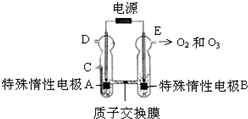 臭氧是一種強氧化劑,常用于消毒、滅菌等.
臭氧是一種強氧化劑,常用于消毒、滅菌等.pH t/min T/℃ | 3,.0 | 4,.0 | 5,.0 | 6,.0 |
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 48 | 15 |
| 50 | 31 | 26 | 15 | 7 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲烷和氯氣反應生成一氯甲烷,與苯和硝酸反應生成硝基苯的反應類型相同 | |
| B. | 蔗糖、麥芽糖的分子式都是C12H22O11,它們互為同分異構體 | |
| C. | “地溝油”可通過水解制得肥皂 | |
| D. | 苯不能使酸性KMnO4溶液褪色,因此苯不能發生氧化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
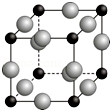 已知A、B、C、D、E、F都是周期表中前四周期的元素,它們的核電荷數依次增大.其中基態A原子價電子排布式為nsnnpn+1;化合物B2E為離子化合物,E原子核外的M層中只有兩對成對電子;C元素是地殼中含量最高的金屬元素;D單質常用于制作太陽能電池和集成電路芯片;F原子最外層電子數與B的相同,其余各內層軌道均充滿電子.請根據以上信息,回答下列問題(答題時,A、B、C、D、E、F用所對應的元素符號表示):
已知A、B、C、D、E、F都是周期表中前四周期的元素,它們的核電荷數依次增大.其中基態A原子價電子排布式為nsnnpn+1;化合物B2E為離子化合物,E原子核外的M層中只有兩對成對電子;C元素是地殼中含量最高的金屬元素;D單質常用于制作太陽能電池和集成電路芯片;F原子最外層電子數與B的相同,其余各內層軌道均充滿電子.請根據以上信息,回答下列問題(答題時,A、B、C、D、E、F用所對應的元素符號表示):查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
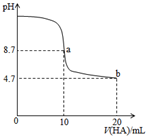 室溫下向10mL0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA溶液,pH的變化曲線如圖所示.下列說法正確的是( )
室溫下向10mL0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA溶液,pH的變化曲線如圖所示.下列說法正確的是( )| A. | a點所示溶液中c(Na+)>c(A-)>c(H+)>c(HA) | |
| B. | a、b兩點所示溶液中水的電離程度相同 | |
| C. | b點所示溶液中c(A-)>c(HA) | |
| D. | 滴定過程中不可能出現c(Na+)>c(OH-)>c(A-)>c(H+) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com