
| A. | MgO+H2SO4═MgSO4+H2O | B. | Na2O+H2O═2NaOH | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | SO3+H2O═H2SO4 |
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲烷的標準燃燒熱為890.3kJ.mol-1,則甲烷燃燒的熱化學方程式可表示為:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ.mol-1 | |
| B. | CO(g)的燃燒熱是283.0 kJ/mol,則CO2(g)═2CO(g)+O2(g)的反應熱△H=+2×283.0 kJ/mol | |
| C. | NaOH和HCl反應的中和熱△H=-57.3kJ/mol,則H2SO4和Ca(OH)2反應的中和熱△H=2×(-57.3)kJ/mol | |
| D. | 500℃、30MPa下,將0.5mol N2和1.5molH2置于密閉的容器中充分反應生成NH3(g),放熱19.3kJ,其熱化學方程式為:N2(g)+3H2(g)$?_{550℃,30Mpa}^{催化劑}$2NH3(g)△H=-38.6kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
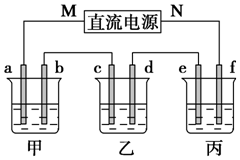 如圖所示裝置中,甲、乙、丙三個燒杯依次分別盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,電極均為石墨電極.
如圖所示裝置中,甲、乙、丙三個燒杯依次分別盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,電極均為石墨電極.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
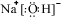 ,并指出其中存在的化學鍵.離子鍵和共價鍵
,并指出其中存在的化學鍵.離子鍵和共價鍵查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
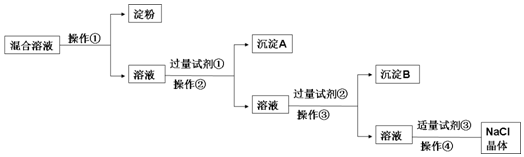
| 編號 | 實驗操作 | 預期現象和結論 |
| ① | ||
| ② |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年甘肅省高二上第一次學段考試化學卷(解析版) 題型:填空題
為了研究碳酸鈣與鹽酸反應的反應速率,某同學通過如圖實驗裝置測定反應中生成的CO2氣體體積,并繪制出如圖所示的曲線。請分析討論以下問題。


(1)化學反應速率最快的時間段是 ,影響此時間段反應速率的主要因素是 ;
A.O~t1 B.t1~t2 C.t2~t3 D.t3~t4
(2)為了減緩上述反應速率,欲向鹽酸中加入下列物質,你認為可行的有 ;
A.蒸餾水 B.NaCl固體 C.NaCl溶液 D.通入HCl
(3)若鹽酸的體積是20 mL,圖中CO2的體積是標準狀況下的體積,則t1~t2時間段平均反應速率v(HCl)= mol·(L·min)-1。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com