
I、煤制天然氣的工藝流程簡圖如下:
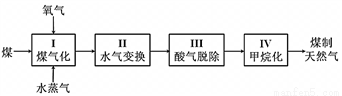
⑴反應I:C(s) + H2O(g) CO(g) + H2(g) ΔH = +135 kJ·mol-1,通入的氧氣會與部分碳發生燃燒反應。請利用能量轉化及平衡移動原理說明通入氧氣的作用:___________________________。
CO(g) + H2(g) ΔH = +135 kJ·mol-1,通入的氧氣會與部分碳發生燃燒反應。請利用能量轉化及平衡移動原理說明通入氧氣的作用:___________________________。
⑵反應II:CO(g) + H2O(g)  CO2(g) + H2(g) ΔH = ?41 kJ·mol-1。如圖表示不同溫度條件下,煤氣化反應I發生后的汽氣比(水蒸氣與CO物質的量之比)與CO平衡轉化率的變化關系。
CO2(g) + H2(g) ΔH = ?41 kJ·mol-1。如圖表示不同溫度條件下,煤氣化反應I發生后的汽氣比(水蒸氣與CO物質的量之比)與CO平衡轉化率的變化關系。
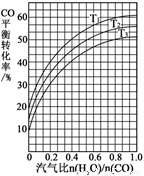
① 判斷T1、T2和T3的大小關系:______________。(從小到大的順序)
② 若煤氣化反應I發生后的汽氣比為0.8,經煤氣化反應I和水氣變換反應II后,得到CO與H2的物質的量之比為1:3,則反應II應選擇的溫度是_______(填“T1”或“T2”或“T3”)。
⑶① 甲烷化反應IV發生之前需要進行脫酸反應III。煤經反應I和II后的氣體中含有兩種酸性氣體,分別是H2S和_______。
② 工業上常用熱碳酸鉀溶液脫除H2S氣體得到兩種酸式鹽,該反應的離子方程式是_______。
II、利用甲烷超干重整CO2技術可得到富含CO的氣體,將甲烷和二氧化碳轉化為可利用的化學品,其能源和環境上的雙重意義重大。該技術中的化學反應為:
CH4 (g)+3CO2 (g) 2H2O(g)+4CO(g)
2H2O(g)+4CO(g)  H>0
H>0
CH4超干重整CO2的催化轉化原理示意如圖:
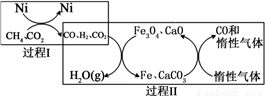
⑷過程II,實現了含氫物種與含碳物種的分離。生成H2O(g)的化學方程式是______________。
⑸假設過程I和過程II中的各步均轉化完全,下列說法正確的是_______。((填序號)
a.過程I和過程II中均含有氧化還原反應
b.過程II中使用的催化劑為Fe3O4 和CaCO3
c.若過程I投料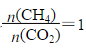 ,可導致過程II中催化劑失效
,可導致過程II中催化劑失效
(6)一定條件下,向體積為2L的恒容密閉容器中充入1.2 mol CH4(g)和4.8 mol CO2(g),發生反應CH4 (g)+3CO2 (g) 2H2O(g)+4CO(g)
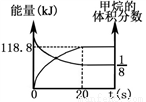
2H2O(g)+4CO(g)  H>0,實驗測得,反應吸收的能量和甲烷的體積分數隨時間變化的曲線圖像如圖。計算該條件下,此反應的
H>0,實驗測得,反應吸收的能量和甲烷的體積分數隨時間變化的曲線圖像如圖。計算該條件下,此反應的 H=________________。
H=________________。
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:2016-2017學年河北省高二下學期第一次月考化學試卷(解析版) 題型:選擇題
綠原酸的結構簡式如下圖,則下列有關綠原酸的說法不正確的是
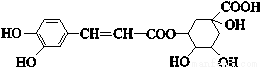
A.分子式為C16H18O9
B.既可以與氫氣發生加成反應,又可以使酸性KMnO4溶液褪色
C.還能發生取代、加聚、消去等反應
D.在鎳做催化劑的情況下,1 mol綠原酸發生加成反應最多可消耗6 mol 氫氣
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖北省沙市高一下學期第三次雙周考(A卷)化學試卷(解析版) 題型:簡答題
碳及其含碳化合物在人們的生產生活中應用廣泛。
(1)將不同量的CO2(g)和H2(g)分別通入到體積為2L的恒容密閉容器中,進行反應2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g),得到如表三組數據;
實驗組 | 溫度℃ | 起始量/mol | 平衡量/mol | 達到平衡所需 時間/min | ||
CO2 | H2 | H2 | C2H5OH | |||
1 | 650 | 2 | 6.8 | 2.0 | 0.8 | 6 |
2 | 900 | 2 | 4.4 | 2.0 | 0.4 | 3 |
3 | 900 | 4 | 8.8 | C | d | t |
①實驗1中以v(H2)表示的反應速率為________________
②已知在一定溫度下,當一個可逆反應達到化學平衡時,生成物濃度冪之積與反應物濃度冪之積的比值是一個常數稱之為化學平衡常數。900℃化學平衡常數為______________,
③如果改變影響平衡的條件之一(如溫度,壓強,反應物的濃度)平衡將向著能夠減弱這種改變的方向移動。則第3組與第2組相比CO2的轉化率___________(填“增大”“減小”“不變” 不能確定).
(2)將CH4設計成燃料電池,其利用率更高,裝置示意如圖(A、B為多孔性碳棒). 持續通入甲烷,在標準狀況下,消耗甲烷體積VL.
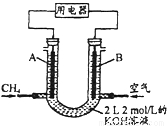
①0<V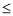 44.8L時,負極電極反應為_________________
44.8L時,負極電極反應為_________________
②44.8L<V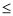 89.6L時,電池總反應方程式為_____________
89.6L時,電池總反應方程式為_____________
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖北省沙市高一下學期第三次雙周考(A卷)化學試卷(解析版) 題型:選擇題
參照反應Br+H2 HBr+H的能量對應反應歷程的示意圖,下列敘述中正確的是( )
HBr+H的能量對應反應歷程的示意圖,下列敘述中正確的是( )

A.正反應為吸熱反應
B.吸熱反應一定要加熱后才能發生
C.反應物總能量高于生成物總能量
D.升高溫度可增大正反應速率,降低逆反應速率
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖北省沙市高一下學期第三次雙周考(A卷)化學試卷(解析版) 題型:選擇題
下列措施不符合節能減排的是 ( )
A.大力發展火力發電,解決電力緊張問題
B.在屋頂安裝太陽能熱水器為居民提供生活用熱水
C.用石灰對煤燃燒后形成的煙氣脫硫,并回收石膏
D.用雜草、生活垃圾等有機廢棄物在沼氣池中發酵產生沼氣,作家庭燃氣
查看答案和解析>>
科目:高中化學 來源:2017屆湖北省八校高三第二次聯考(3月)理綜化學試卷(解析版) 題型:選擇題
分子式為C4H8O的三元環同分異構體共有(不考慮立體異構)( )
A. 5種 B. 6種 C. 7種 D. 8種
查看答案和解析>>
科目:高中化學 來源:2016-2017學年寧夏銀川市高二下學期第一次月考化學試卷(解析版) 題型:填空題
(6分)現有下列幾種常見的物質:①N2 ②NaCl ③Ca(OH)2 ④金剛石⑤SiC ⑥NH3
⑦NH4Cl ⑧CO2。其中,(以下空格均填寫序號)
(1)含有非極性鍵的分子晶體是 ;
(2)含有極性鍵的分子晶體是 ;
(3)只含離子鍵的離子晶體是 ;
(4)含有極性共價鍵的原子晶體是 ;
(5)既含有離子鍵,又含有極性共價鍵和配位鍵的離子晶體是 。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年寧夏銀川市高二下學期第一次月考化學試卷(解析版) 題型:選擇題
已知某離子晶體晶胞如下圖所示,其摩爾質量為M,阿伏加德羅常數為NA,晶體的密度為d g/cm3。下列說法中正確的是
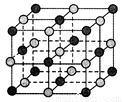
A. 晶體晶胞中陰、陽離子的個數都為1
B. 該晶體中兩個距離最近的同種離子的核間距為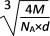 cm
cm
C. 其中陰、陽離子的配位數都是4
D. 該晶胞可能是NaCl的晶胞
查看答案和解析>>
科目:高中化學 來源:2017屆吉林省高三第五次摸底考試理綜化學試卷(解析版) 題型:選擇題
a、b、c、d為短周期元素,a的原子中只有1個電子,b與a可形成多種有機化合物,c的單質是構成空氣的主要成分,d元素的焰色反應呈黃色。下列敘述錯誤的是
A. 簡單離子半徑:c>d
B. a、b、c、d中,d的原子半徑最大
C. a與b、c形成的化合物可能含有非極性鍵
D. a與其它元素形成的化合物均為共價化合物
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com