
分析 (1)根據氧化還原反應中氧化劑的氧化性大于氧化產物的氧化性進行比較;
(2)具有強氧化性的物質能漂白,具有吸附性或能與有色物質反應生成無色物質的均能漂白;
(3)反應中I元素的化合價升高,Br元素的化合價降低,根據得失電子守恒和原子守恒配平方程式.
解答 解:(1)①KBrO3能把KI氧化成I2或KIO3,KBrO3本身被還原為Br2,則氧化性順序是:KIO3<KBrO3,②Br2能把I-氧化為I2,氧化性是I2<Br2,
③KIO3能把I-氧化為I2,氧化性是:I2<KIO3,④KIO3能把Br-氧化為Br2,氧化性是:Br2<KIO3,綜上氧化性順序是:I2<Br2<KIO3<KBrO3,
故答案為:I2<Br2<KIO3<KBrO3;
(2)已知KBrO3具有強氧化性,具有強氧化性的物質能漂白;活性炭具有吸附性能漂白有色物質,二氧化硫能與有色物質反應生成無色物質,所以能漂白;
故答案為:KBrO3具有強氧化性;二氧化硫、活性炭;
(3)KI與KBrO3溶液反應生成I2、Br2,反應中I元素的化合價升高,Br元素的化合價降低,其反應的方程式為:10KI+2KBrO3+6H2SO4=K2SO4+5I2+Br2+6H2O;
故答案為:10KI+2KBrO3+6H2SO4=K2SO4+5I2+Br2+6H2O.
點評 本題考查了氧化還原反應,涉及氧化性強弱的判斷以及電子守恒、元素守恒的應用等知識,注意知識的遷移和應用是關鍵,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | X與Y形成原子個數比1:1的化合物只有2種 | |
| B. | Y、W的氧化物均為酸性氧化物 | |
| C. | 最高價氧化物對應水化物的酸性:Y<W | |
| D. | X與Z形成的化合物中,各原子均滿足8電子穩定結構 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | KNO3溶液 | B. | NaCl溶液 | C. | 銅粉 | D. | 硫酸銅晶體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
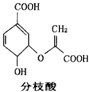
| A. | 可與乙醇、乙酸反應,且反應類型相同 | |
| B. | 1 mo1分枝酸最多可與3 mol NaOH發生中和反應 | |
| C. | 分枝酸的分子式為C10H8O6 | |
| D. | 分枝酸分子中含有2種官能團 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com