
分析 寫出目標反應的方程式,然后根據蓋斯定律及已知熱化學方程式計算出目標反應的反應熱,再寫出目標反應的熱化學方程式.
解答 解:①4Na(g)+3CO2(g)=2Na2CO3(l)+C(s,金剛石)△H=-1080.9kJ/mol,
②4Na(g)+CO2(g)=2Na2O(s)+C(s,金剛石)△H=-357.5kJ/mol,
根據蓋斯定律,①-②×3可得:6Na2O(s)+2C(s,金剛石)=8Na(g)+2Na2CO3(l)△H=-8.4kJ/mol,
故答案為:6Na2O(s)+2C(s,金剛石)=8Na(g)+2Na2CO3(l)△H=-8.4kJ/mol.
點評 本題考查了用蓋斯定律進行有關反應熱的計算,題目難度中等,注意掌握蓋斯定律的概念及含義,明確熱化學方程式的書寫原則,試題培養了學生靈活應用基礎知識的能力.


 導學教程高中新課標系列答案
導學教程高中新課標系列答案 小學課時特訓系列答案
小學課時特訓系列答案科目:高中化學 來源: 題型:選擇題
| A. | NO2、SO2、BF2、NCl3分子中沒有一個分子中原子的最外層電子都滿足了8電子穩定結構 | |
| B. | P4和CH4都是正四面體分子且鍵角都為109°28ˊ | |
| C. | NaCl晶體中與每個Na+距離相等且最近的Na+共有8個 | |
| D. | 單質的晶體中一定不存在的微粒是陰離子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ② | C. | ②③ | D. | ④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{a}{b}$ | B. | $\frac{a}{a+b}$ | C. | $\frac{a}{a+2b}$ | D. | $\frac{a}{2a+b}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 雙氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O | |
| B. | 向明礬溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ | |
| C. | 用銅作電極電解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;電解\;}}{\;}$2Cu+O2↑+4H+ | |
| D. | 氯化鈉與濃硫酸混合加熱:H2SO4+2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$SO2↑+Cl2↑+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | HCl的電子式H:Cl | B. | HClO的結構式H-Cl-O | ||
| C. | Cl-的結構示意圖 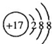 | D. | 質量數為37的氯原子${\;}_{17}^{37}Cl$ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com