
【題目】已知:一元弱酸HA的電離平衡常數K =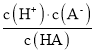 。25℃時,CH3COOH、HCN、H2CO3的電離平衡常數如下:
。25℃時,CH3COOH、HCN、H2CO3的電離平衡常數如下:
化學式 | CH3COOH | HCN | H2CO3 |
K | 1.75×10–5 | 4.9×10–10 | K1 = 4.4×10–7 K2 = 5.6×10–11 |
下列說法正確的是
A. 稀釋CH3COOH溶液的過程中,n(CH3COO–)逐漸減小
B. NaHCO3溶液中:c(H2CO3) < c(![]() ) < c(HCO3)
) < c(HCO3)
C. 25℃時,相同物質的量濃度的NaCN溶液的堿性強于CH3COONa溶液
D. 向CH3COOH溶液或HCN溶液中加入Na2CO3溶液,均產生CO2
【答案】C
【解析】
A.加水稀釋CH3COOH溶液,促進CH3COOH的電離,溶液中n(CH3COO–)逐漸增多,故A錯誤;B.NaHCO3溶液中HCO3-的水解常數Kh2=![]() =
=![]() =2.27×10–8>K2 = 5.6×10–11,說明HCO3-的水解大于電離,則溶液中c(
=2.27×10–8>K2 = 5.6×10–11,說明HCO3-的水解大于電離,則溶液中c(![]() )<c(H2CO3)< c(HCO3),故B錯誤;C.由電離平衡常數可知濃度相等時HCN的酸性小于CH3COOH,同CN-的水解程度大于CH3COO-,則25℃時,相同物質的量濃度的NaCN溶液的堿性強于CH3COONa溶液,故C正確;D.由電離平衡常數可知濃度相等時HCN的酸性小于H2CO3,則向HCN溶液中加入Na2CO3溶液,只能生成NaHCO3,無CO2氣體生成,故D錯誤;故答案為C。
)<c(H2CO3)< c(HCO3),故B錯誤;C.由電離平衡常數可知濃度相等時HCN的酸性小于CH3COOH,同CN-的水解程度大于CH3COO-,則25℃時,相同物質的量濃度的NaCN溶液的堿性強于CH3COONa溶液,故C正確;D.由電離平衡常數可知濃度相等時HCN的酸性小于H2CO3,則向HCN溶液中加入Na2CO3溶液,只能生成NaHCO3,無CO2氣體生成,故D錯誤;故答案為C。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】短周期元素X、Y、Z、W在元素周期表中的相對位置如下圖所示,其中W原子的質子數是其最外層電子數的三倍,下列說法不正確的是( )

A. 原子半徑:W>Z>Y>X
B. 最高價氧化物對應水化物的酸性:X>W>Z
C. 最簡單氣態氫化物的熱穩定性:Y>X>W>Z
D. 元素X、Z、W的最高化合價分別與其主族序數相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎳的單質、合金及其化合物用途非常廣泛。
(1)Ni2+基態核外電子排布式為________。
(2)膠狀鎳可催化CH2=CHC≡N加氫生成CH3CH2C≡N。CH2=CHC≡N分子中σ鍵與π鍵的數目比n(σ)∶n(π)=________;CH3CH2C≡N分子中碳原子軌道的雜化類型為________。
(3)[Ni(N2H4)2](N3)2是一種富氮含能材料。配體N2H4能與水混溶,除因為它們都是極性分子外,還因為______________________;[Ni(N2H4)2]2+中含四個配位鍵,不考慮空間構型,[Ni(N2H4)2]2+的結構可用示意圖表示為______________________。
(4)一種新型的功能材料的晶胞結構如下圖所示,它的化學式可表示為________。
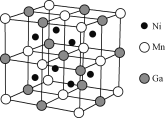
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】1,2-二氯丙烷(CH2C1CHClCH3)是一種重要的化工原料,工業上可用丙烯加成法制備,主要副產物為3-氯丙烯(CH2=CHCH2C1),反應原理為:
I.CH2=CHCH3(g)+C12(g)![]() CH2C1CHC1CH3(g) △H1=—134kJ·mol-1
CH2C1CHC1CH3(g) △H1=—134kJ·mol-1
II.CH2=CHCH3(g)+C12(g)![]() CH2=CHCH2C1(g)+HC1(g)△H2=—102kJ·mol-1
CH2=CHCH2C1(g)+HC1(g)△H2=—102kJ·mol-1
請回答下列問題:
(1)已知CH2=CHCH2C1(g)+HC1(g)![]() CH2C1CHC1CH3(g)的活化能Ea(正)為132kJ·mol-1,則該反應的活化能Ea(逆)為______kJ·mol-1。
CH2C1CHC1CH3(g)的活化能Ea(正)為132kJ·mol-1,則該反應的活化能Ea(逆)為______kJ·mol-1。
(2)一定溫度下,向恒容密閉容器中充入等物質的量的CH2=CHCH3(g)和C12(g)。在催化劑作用下發生反應I、Ⅱ,容器內氣體的壓強隨時間的變化如下表所示。
時間/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
壓強/kPa | 80 | 74.2 | 69.4 | 65.2 | 61.6 | 57.6 | 57.6 |
①用單位時間內氣體分壓的變化來表示反應速率,即![]() ,則前120min內平均反應速率v(CH2C1CHC1CH3)=______kPa·min-1。(保留小數點后2位)。
,則前120min內平均反應速率v(CH2C1CHC1CH3)=______kPa·min-1。(保留小數點后2位)。
②該溫度下,若平衡時HC1的體積分數為![]() ,則丙烯的平衡總轉化率
,則丙烯的平衡總轉化率![]() _______;反應I的平衡常數Kp=_____kPa-1(Kp為以分壓表示的平衡常數,保留小數點后2位)。
_______;反應I的平衡常數Kp=_____kPa-1(Kp為以分壓表示的平衡常數,保留小數點后2位)。
(3)某研究小組向密閉容器中充入一定量的CH2=CHCH3和C12,分別在A、B兩種不同催化劑作用下發生反應,一段時間后測得CH2C1CHC1CH3的產率與溫度的關系如下圖所示。
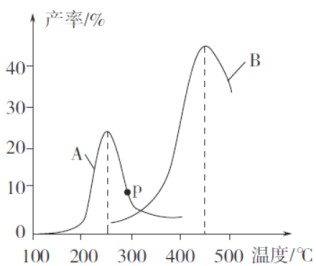
①下列說法錯誤的是___________(填代號)。
a.使用催化劑A的最佳溫度約為250℃
b.相同條件下,改變壓強不影響CH2C1CHC1CH3的產率
c.兩種催化劑均能降低反應的活化能,但△H不變
d.提高CH2C1CHC1CH3反應選擇性的關鍵因素是控制溫度
②在催化劑A作用下,溫度低于200℃時,CH2C1CHC1CH3的產率隨溫度升高變化不大,主要原因是_______________________________________________________________。
③p點是否為對應溫度下CH2C1CHC1CH3的平衡產率,判斷理由是_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甘氨酸亞鐵[(NH2CH2COO)2Fe]是一種補鐵強化劑。實驗室利用FeCO3與甘氨酸(NH2CH2COOH)制備甘氨酸亞鐵,實驗裝置如下圖所示(夾持和加熱儀器已省略)。
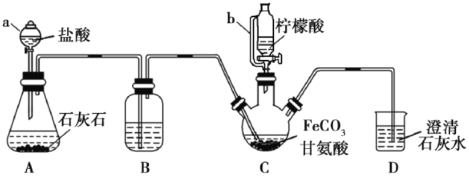
查閱資料:
①甘氨酸易溶于水,微溶于乙醇;甘氨酸亞鐵易溶于水,難溶于乙醇。
②檸檬酸易溶于水和乙醇,具有較強的還原性和酸性。
實驗過程:
I.裝置C中盛有17.4gFeCO3和200mL1.0mol·L-1甘氨酸溶液。實驗時,先打開儀器a的活塞,待裝置c中空氣排凈后,加熱并不斷攪拌;然后向三頸瓶中滴加檸檬酸溶液。
Ⅱ.反應結束后過濾,將濾液進行蒸發濃縮;加入無水乙醇,過濾、洗滌并干燥。
(1)儀器a的名稱是________;與a相比,儀器b的優點是_______________。
(2)裝置B中盛有的試劑是:____________;裝置D的作用是________________。
(3)向FeSO4溶液中加入NH4HCO3溶液可制得FeCO3,該反應的離子方程式為____________________________。
(4)過程I加入檸檬酸促進FeCO3溶解并調節溶液pH,溶液pH與甘氨酸亞鐵產率的關系如圖所示。
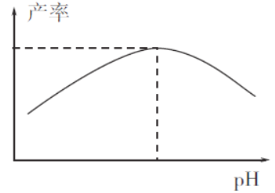
①pH過低或過高均導致產率下降,其原因是_____________________;
②檸檬酸的作用還有________________________。
(5)過程II中加入無水乙醇的目的是_______________________。
(6)本實驗制得15.3g甘氨酸亞鐵,則其產率是_____%。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列溶液或濁液中,關于離子濃度的說法正確的是
A. 一定濃度的氨水加水稀釋的過程中,c(NH4+)/ c(NH3·H2O)的比值減小
B. 濃度均為0.1 mol·L-1的Na2CO3、NaHCO3混合溶液中:c(CO32-)< c(HCO3-),且3c(Na+)=2[c(CO32-)+c(HCO3-+ c(H2CO3)]
C. 0.2 mol·L-1的醋酸(CH3COOH)溶液與0.1 mol·L-1 NaOH溶液等體積混合后:c(CH3COO-) + 2c(OH-)=c(CH3COOH) + 2c(H+)
D. 常溫下,已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2Cr2O4)=2.0×10-12,則Ag2CrO4懸濁液中的c(Ag+)一定小于AgCl懸濁液中的c(Ag+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】納米級Fe3O4可用于以太陽能為熱源分解水制H2,過程如下圖所示。下列說法正確的是:

A.過程Ⅰ的反應為6FeO+O2![]() 2Fe3O4
2Fe3O4 ![]()
B.過程Ⅱ中H2為還原劑
C.整個過程的總反應為:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
D.FeO是過程Ⅰ的氧化產物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組同學研究SO2和KI溶液的反應,設計如下實驗。
實驗 | 操作 | 現象 |
I |
| 溶液迅速變為淺黃色,將溶液進行離心分離無固體沉積, 加入淀粉溶液,不變色 |
II |
| 溶液立即變成深黃色,將溶液進行離心分離有淺黃色固體沉積,溶液黃色變淺,加入淀粉溶液,不變色 |
(1)加入淀粉溶液的目的是______,為達到相同的目的,還可選用的試劑是______。
(2)經檢驗,II中的淺黃色固體是硫。資料顯示,在酸性條件下,SO2和KI溶液反應生成S和I2。
① 在酸性條件下,SO2和KI溶液反應的離子方程式是______。
② 針對II中加入淀粉溶液不變色,甲同學提出假設:______。為證實該假設,甲同學取II中離心分離后的溶液,加入鹽酸酸化的BaCl2溶液,有白色沉淀生成。
③ 乙同學認為甲同學的實驗方案不支持上述假設,理由是______。
④ 丙同學向1 mL 1 mol·L1 KCl溶液中加入5滴1 mol·L1鹽酸,通入SO2,無明顯實驗現象,再加入鹽酸酸化的BaCl2溶液,幾乎沒有白色沉淀。丙同學的實驗結論是______。
(3)實驗表明,I是SO2轉化的催化劑。補全下列離子方程式。
SO2+H2O ===_____ + +
(4)對比實驗I和II,推測增大H+的濃度可加快SO2的轉化速率。為證實該推測,還需進一步進行實驗證明,實驗方案是______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關說法正確的是 ( )
A. 反應NH3(g)+HCl(g)=NH4Cl(s)在室溫下可自發進行,則該反應的△H<0
B. 所有的化學反應都需要一定的活化能來推動
C. CH3COOH 溶液加水稀釋后,溶液中![]() 的值增大
的值增大
D. Na2CO3溶液中加入少量Ca(OH)2 固體,CO32-水解程度減小,溶液的pH 減小
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com