
| 13.44L |
| 22.4L/mol |
| 0.2mol×108g/mol |
| 60g |
| 0.6mol×2+0.2mol×1 |
| 4 |


 陽光試卷單元測試卷系列答案
陽光試卷單元測試卷系列答案科目:高中化學 來源: 題型:
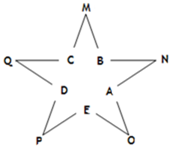 今有A、B、C、D、E五種常見單質,且相鄰的單質可生成對應的化合物M、N、O、P、Q(反應關系如圖所示),常溫下A呈氣態,其余均為固態,N分子中各原子均滿足八電子穩定結構;又知過量B與A作用產生白霧,B與過量A作用產生白煙;E在A中燃燒產生棕色的煙;Q遇水立刻水解產生白色絮狀沉淀和氣體,該沉淀能溶于氫氧化鈉溶液但不溶于氨水;P為黑色固體且能溶于稀鹽酸.試回答下列問題:
今有A、B、C、D、E五種常見單質,且相鄰的單質可生成對應的化合物M、N、O、P、Q(反應關系如圖所示),常溫下A呈氣態,其余均為固態,N分子中各原子均滿足八電子穩定結構;又知過量B與A作用產生白霧,B與過量A作用產生白煙;E在A中燃燒產生棕色的煙;Q遇水立刻水解產生白色絮狀沉淀和氣體,該沉淀能溶于氫氧化鈉溶液但不溶于氨水;P為黑色固體且能溶于稀鹽酸.試回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
| A、原子半徑大小:Z>Y>X>W |
| B、Y、Z兩種元素的氧化物對應的水化物酸性為:Y<Z |
| C、X、Y、Z三種元素的單質均既有氧化性又有還原性 |
| D、W、Y、Z三種元素形成的氣態氫化物中最穩定的是Z的氣態氫化物 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、1Llmol/L的Na2CO3溶液中含有的CO32-數目為NA |
| B、1mol羥基(-OH)所含的電子數約為l0NA |
| C、1mol丙烯分子有2molσ鍵,1molπ鍵 |
| D、現有乙烯、丙烯、丁烯的混合氣體共14g,其原子數為3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:
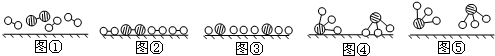
 、
、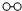 、
、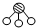 分別表示N2、H2、NH3.圖⑤表示生成的NH3離開催化劑表面.分別寫出圖②→③、圖③→④表示的變化過程
分別表示N2、H2、NH3.圖⑤表示生成的NH3離開催化劑表面.分別寫出圖②→③、圖③→④表示的變化過程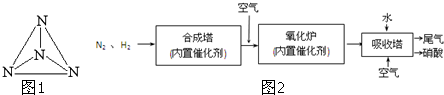
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、一定含甲烷,不含乙烷 |
| B、一定含乙烷,不含甲烷 |
| C、可能是甲烷和乙烯的混合物 |
| D、一定含甲烷,但不含乙烯 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、4.6mol/L |
| B、3.2mol/L |
| C、2.5mol/L |
| D、1.2mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、1 molCH5+所含的電子數為10NA |
| B、1 molC20H42中含有61 NA個共價鍵 |
| C、25℃時1 mL純水中含有10-10NA個OH-離子 |
| D、22.4 L的NH3中含有4 NA個原子 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com