
分析 (1)鎂能在二氧化碳中燃燒;
(2)酸性環境下過氧化氫氧化銅生成銅離子;
(3)NaAlO2溶液中通入過量的CO2反應生成氫氧化鋁和碳酸氫鈉,以此來解答;
(4)鐵離子水解生成膠體,可凈化水;酸性溶液中抑制鐵離子的水解,酸性條件下亞鐵離子與重鉻酸根離子發生氧化還原反應,以此來解答;
(5)與量有關的反應,現象不同,可利用相互滴加的實驗方法鑒別,以此來解答.
解答 解:(1)鎂能在二氧化碳中燃燒,化學方程式為:2Mg+CO2$\frac{\underline{\;點燃\;}}{\;}$2MgO+C,故答案為:2Mg+CO2$\frac{\underline{\;點燃\;}}{\;}$2MgO+C;
(2)用H2O2和稀H2SO4的混合溶液可溶出印刷電路板金屬粉末中的銅,反應生成硫酸銅和水,化學方程式:Cu+H2SO4+H2O2═CuSO4+2H2O;
故答案為:Cu+H2SO4+H2O2═CuSO4+2H2O;
(3)NaAlO2溶液中通入過量的CO2反應生成氫氧化鋁和碳酸氫鈉,離子反應為AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,
故答案為:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-;
(4)Fe2(SO4)3 凈水的原理是Fe3++3H2O?Fe(OH)3(膠體)+3H+,生成的少量Fe(OH)3膠體可以吸附水中的懸浮雜質,達到凈水的目的;
使用時發現Fe2(SO4)3 并不能使酸性廢水中的懸浮物沉降除去,其原因是因為在酸性廢液中,H+會抑制Fe3+的水解,無法得到Fe(OH)3膠體,所以不能夠吸附懸浮物;
在酸性環境下,向含重鉻酸根的廢水中加入FeSO4溶液,然后調節pH,使生成的Cr3+轉化為Cr(OH)3,第一步反應的離子方程式為Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,
故答案為:Fe3++3H2O?Fe(OH)3(膠體)+3H+,生成的少量Fe(OH)3膠體可以吸附水中的懸浮雜質,達到凈水的目的;因為在酸性廢液中,H+會抑制Fe3+的水解,無法得到Fe(OH)3膠體,所以不能夠吸附懸浮物;Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O;
(5)①硫酸鋁和氨水的反應與量無關,改變滴加順序均生成白色沉淀,不能鑒別,故不選;
②偏鋁酸鈉和稀鹽酸反應與量有關,鹽酸足量不生成沉淀,鹽酸少量生成白色沉淀,改變滴加順序現象不同,能鑒別,故選;
③硫酸鋅和氫氧化鈉的反應與量有關,NaOH不足生成白色沉淀,NaOH過量沉淀溶解,改變滴加順序現象不同,能鑒別,故選;
④硫酸鋅和氨水的反應與量有關,氨水不足生成白色沉淀,氨水過量沉淀溶解,改變滴加順序現象不同,能鑒別,故選;
故答案為:②③④.
點評 本題考查物質的鑒別和檢驗,為高頻考點,把握物質的性質、發生的反應及現象為解答的關鍵,側重分析與實驗能力的考查,注意習題信息及元素化合物知識的應用,題目難度不大.


 輕松課堂單元期中期末專題沖刺100分系列答案
輕松課堂單元期中期末專題沖刺100分系列答案科目:高中化學 來源:2016-2017學年江蘇省徐州市高一上第一次月考化學卷(解析版) 題型:選擇題
如圖是課外活動小組設計的用化學電源使LED燈發光的裝置。下列說法錯誤的是
A.銅片表面有氣泡生成
B.裝置中存在“化學能→ 電能→ 光能”的轉換
C.如果將硫酸換成檸檬汁,導線中不會有電子流動
D.如果將鋅片換成鐵片,電路中的電流方向不變
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
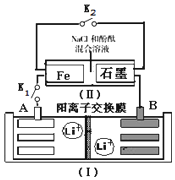 如圖裝置(Ⅰ)為一種可充電鋰離子電池的示意圖,該電池充、放電的化學方程式為:Li4Ti5O12+3Li$?_{充電}^{放電}$ Li7Ti5 O12.裝置(Ⅱ)為電解池的示意圖.當閉合K1,斷開K2時,Fe電極附近溶液先變紅.下列說法正確的是( )
如圖裝置(Ⅰ)為一種可充電鋰離子電池的示意圖,該電池充、放電的化學方程式為:Li4Ti5O12+3Li$?_{充電}^{放電}$ Li7Ti5 O12.裝置(Ⅱ)為電解池的示意圖.當閉合K1,斷開K2時,Fe電極附近溶液先變紅.下列說法正確的是( )| A. | 閉合K1,斷開K2時,若將Fe電極和石墨電極互換,裝置(Ⅱ)中發生的總反應為:2NaCl+2H2O$\frac{\underline{\;電解\;}}{\;}$2NaOH+Cl2↑+H2↑ | |
| B. | 閉合K1,斷開K2時,當0.1 mol Li+從A極區遷移到B極區,理論上Fe電極上產生的氣體體積為1.12 L(標準狀況下) | |
| C. | 取下鋰離子電池充電,電極A為陽極,發生還氧化反應,電極上發生的電極反應式為:Li7Ti5O12-3e-═Li4Ti5O12+3 Li+ | |
| D. | 若開始時,斷開K1,閉合K2,一段時間后,石墨電極附近顯紅色,則該電極反應為:2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4LH2O含有的分子數為 NA | |
| B. | 常溫常壓下,1.06g Na2CO3含有的Na+離子數為0.02 NA | |
| C. | 通常狀況下,NA 個CO2分子占有的體積為22.4L | |
| D. | 物質的量為0.5 mol的MgCl2中,含有Mg2+個數為 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 空氣、硫酸銅、H2SO4 | B. | HCl、Fe(OH)3膠體、純堿 | ||
| C. | 二氧化碳、膽礬、氫氧化鉀 | D. | HNO3、食鹽水、燒堿 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.0mol•L-1KNO3溶液:H+、Fe2+、SCN-、SO42- | |
| B. | 中性溶液:Fe3+、K+、Cl-、SO42- | |
| C. | c(H+)/c(OH-)=10-10的溶液:Ba2+、NO3-、Cl- | |
| D. | c(ClO-)=1.0mol•L-1的溶液:Na+、SO32-、S2-、SO42- |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省高二上第一次月考化學試卷(解析版) 題型:選擇題
下列說法正確的是( )
A.增大反應物濃度,可增大單位體積內活化分子的百分數,從而使有效碰撞次數增大
B.有氣體參加的化學反應,若增大壓強(即縮小反應容器的體積),可增加活化分子的百分數,從而使反應速率增大
C.升高溫度能使化學反應速率增大,主要原因是增加了反應物分子中活化分子的百分數
D.催化劑不影響反應活化能但能增大單位體積內活化分子百分數,從而增大反應速率
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com