
| A. | 實驗①生成的氣體不能使濕潤的KI-淀粉試紙變藍 | |
| B. | 實驗②證明Fe2+既有氧化性又有還原性 | |
| C. | 上述實驗證明氧化性:MnO4->CI2>Fe3+>I2 | |
| D. | 上述實驗中,共有兩個氧化還原反應 |
分析 ①向KMnO4晶體滴加濃鹽酸,產生黃綠色氣體,該反應中Mn元素化合價由+7價變為+2價、Cl元素化合價由-1價變為0價,高錳酸鉀是氧化劑、濃鹽酸是還原劑;
②向FeCl2溶液中通入少量氯氣,溶液變黃色,鐵元素化合價由+2價變為+3價、Cl元素化合價由0價變為-1價,氯化亞鐵是還原劑、氯氣是氧化劑;
③取實驗②生成的溶液滴在淀粉KI試紙上,試紙變藍色,鐵離子和碘離子發生氧化還原反應生成碘和亞鐵離子,I元素化合價由-1價變為0價、鐵元素化合價由+3價變為+2價,所以碘離子作還原劑、鐵離子為氧化劑.
解答 解:①向KMnO4晶體滴加濃鹽酸,產生黃綠色氣體,該反應中Mn元素化合價由+7價變為+2價、Cl元素化合價由-1價變為0價,高錳酸鉀是氧化劑、濃鹽酸是還原劑,氧化性:MnO4->Cl2;
②向FeCl2溶液中通入少量氯氣,溶液變黃色,鐵元素化合價由+2價變為+3價、Cl元素化合價由0價變為-1價,氯化亞鐵是還原劑、氯氣是氧化劑,氧化性:Cl2>Fe3+;
③取實驗②生成的溶液滴在淀粉KI試紙上,試紙變藍色,鐵離子和碘離子發生氧化還原反應生成碘和亞鐵離子,I元素化合價由-1價變為0價、鐵元素化合價由+3價變為+2價,所以碘離子作還原劑、鐵離子為氧化劑,氧化性:Fe3+>I2.
A.氧化性:Cl2>Fe3+,鐵離子能把碘離子氧化為單質碘,所以氯氣也能氧化碘離子,即氯氣能使濕潤的KI-淀粉試紙變藍,故A錯誤;
B.鐵元素化合價由+2價變為+3價,氯化亞鐵是還原劑,說明Fe2+具有還原性,所以上述實驗不能證明Fe2+具有氧化性,故B錯誤;
C.通過以上分析知,上述實驗證明氧化性:MnO4->Cl2>Fe3+>I2,故C正確;
D.上述三個實驗中,共有三個氧化還原反應,故D錯誤,
故選C.
點評 本題考查了氧化還原反應,根據反應中元素化合價變化結合基本概念來分析解答,題目難度不大,側重于考查學生對基礎知識的應用能力.


科目:高中化學 來源: 題型:選擇題
| A. | 僅由碳、氫兩種元素組成 | B. | 僅由碳、氫、氧三種元素組成 | ||
| C. | 在氧氣中燃燒只生成二氧化碳 | D. | 熔點低而且難溶于水 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

| 操作步驟 | 實驗現象 | 解釋原因 |
 | 滴加硝酸銀溶液,現象有:產生白色沉淀 | 原因有:氯氣與水反應后,電離出Cl-,Cl-與Ag+生成AgCl白色沉淀 |
 | 滴加紫色石蕊試液,現象有:先變紅,后褪色 | 原因有:氯氣與水反應后,溶液顯酸性使紫色石蕊試液變紅,產生的HClO又使紅色的石蕊試液發生漂白 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
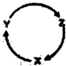 如表各組物質中,不能通過一步反應實現如圖所示轉化的是( )
如表各組物質中,不能通過一步反應實現如圖所示轉化的是( )| 選項 | X | Y | Z |
| A | Fe | FeCl3 | FeCl2 |
| B | NH4Cl | NH3 | NO |
| C | C | CO | CO2 |
| D | Al2O3 | AlCl3 | Al(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
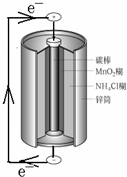
| A. | 鋅筒作負極,發生氧化反應 | |
| B. | 電子從鋅流向碳棒,碳棒得電子被還原 | |
| C. | 電池內部的NH4+向碳棒移動 | |
| D. | 將NH4Cl更換為KOH能提高電池壽命和性能 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
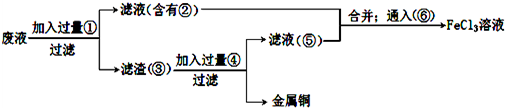
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | [Cr(H2O)6]Cl3 | B. | [Cr(H2O)5Cl]Cl2•H2O | ||
| C. | [Cr(H2O)4Cl2]Cl•2H2O | D. | [Cr(H2O)3Cl3]•3H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com