
【題目】(1)![]() X表示原子:
X表示原子:
①AXn+共有x個電子,則該陽離子的中子數N=____。
②12C16O2分子中的中子數N=______。
③A2-原子核內有x個中子,其質量數為m,則n g A2-所含電子的物質的量為_____。
(2)某元素原子的核電荷數是電子層數的5倍,其質子數是最外層電子數的3倍,該元素的原子結構示意圖是_____。
(3)已知某粒子的結構示意圖為![]()
試回答:①當x-y=10時,該粒子為___(填“原子”、“陽離子”或“陰離子”)。
②寫出y=3與y=7的元素最高價氧化物對應水化物發生反應的離子方程式_____。
【答案】A-x-n 22 ![]() mol
mol ![]() 原子 Al(OH)3+3H+=Al3++3H2O
原子 Al(OH)3+3H+=Al3++3H2O
【解析】
(1)根據“質子數+中子數=質量數”的關系,
①AXn+共有x個電子,中性原子X的電子數為x+n,則N=A-x-n;
②12C16O2分子中的中子數為6+8+8=22;
③A2-所含電子數為m-x+2,則n g A2-所含電子的物質的量為![]() mol。
mol。
(2)設核電荷數=質子數=a,元素原子的電子層數為x,最外層電子數為y,依題意:a=5x,a=3y,則5x=3y,x=![]() ,因原子的最外層電子數不超過8,即y為1~8的正整數,故僅當y=5,x=3合理,該元素的核電荷數為15,則該元素的原子結構為
,因原子的最外層電子數不超過8,即y為1~8的正整數,故僅當y=5,x=3合理,該元素的核電荷數為15,則該元素的原子結構為![]() ;
;
(3)①當x-y=10時,x=10+y,說明核電荷數等于核外電子數,所以該粒子應為原子;
②y=3時,該微粒為鋁原子,y=7時,該微粒為氯原子,其最高價氧化物對應的水化物分別為氫氧化鋁和高氯酸,反應的離子方程式為Al(OH)3+3H+=Al3++3H2O。


 尖子生新課堂課時作業系列答案
尖子生新課堂課時作業系列答案 英才計劃同步課時高效訓練系列答案
英才計劃同步課時高效訓練系列答案科目:高中化學 來源: 題型:
【題目】如圖是金屬鎂和鹵素單質(X2)反應的能量變化示意圖.下列說法正確的是( )
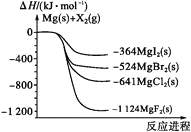
A. 由MgCl2制取Mg是放熱過程
B. 熱穩定性:MgI2>MgBr2>MgCl2>MgF2
C. 常溫下氧化性:F2<Cl2<Br2<I2
D. 由圖可知此溫度下MgBr2(s)與Cl2(g)反應的熱化學方程式為:MgBr2(s) + Cl2(g) ═ MgCl2(s) + Br2(g) △H = -117kJ/mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在20世紀90年代末期,科學家發現并證明碳有新的單質形態![]() 存在。后來人們又相繼得到了
存在。后來人們又相繼得到了![]() 、
、![]() 、
、![]() 、
、![]() 等另外一些球碳分子。21世紀初,科學家又發現了管狀碳分子和洋蔥狀碳分子,大大豐富了碳元素單質的家族。下列有關說法錯誤的是
等另外一些球碳分子。21世紀初,科學家又發現了管狀碳分子和洋蔥狀碳分子,大大豐富了碳元素單質的家族。下列有關說法錯誤的是

A. 熔點比較: ![]()
B. ![]() 、
、![]() 、管狀碳和洋蔥狀碳之間的轉化屬于化學變化
、管狀碳和洋蔥狀碳之間的轉化屬于化學變化
C. ![]() 晶體結構如上圖所示,每個
晶體結構如上圖所示,每個![]() 分子周圍與它最近且等距離的
分子周圍與它最近且等距離的![]() 分子有12個
分子有12個
D. ![]() 、
、![]() 、管狀碳和洋蔥狀碳都不能與
、管狀碳和洋蔥狀碳都不能與![]() 發生反應
發生反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋅錳干電池是最早的實用電池。現用下列工藝回收正極材料中的金屬(部分條件未給出)。

(1)堿性鋅錳電池反應為:Zn+2MnO2+2H2O=Zn(OH)2+2MnO(OH),電解質是KOH, MnO(OH)中Mn的化合價為:_____,正極反應式為:__________。
(2)黑粉的主要成份為 MnO2和石墨,寫出反應①的化學方程式:________
(3)MnO2的轉化率與溫度的關系如下表:
溫度/℃ | 20 | 40 | 60 | 80 | 100 |
轉化率/℃ | 86.0 | 90.0 | 91.3 | 92.0 | 92.1 |
生產中常選反應溫度為80℃,其理由是:___________。
(4)“沉錳”過程中生成堿式碳酸錳[MnCO36Mn(OH)25H2O],寫出其離子反應方程式:_______。濾液③中可回收的物質為:________(填化學式)。
(5)用硫酸酸化的![]() 漿液可吸收工業廢氣中的
漿液可吸收工業廢氣中的![]() 生成
生成![]() ,已知漿液中
,已知漿液中![]() 含量為
含量為![]() ,工業廢氣中
,工業廢氣中![]() 含量為
含量為![]() ,
, ![]() 的吸收率可達90%,則處理1000
的吸收率可達90%,則處理1000![]() 工業尾氣,可得到
工業尾氣,可得到![]() 的質量為____kg(用含字母的代數式表示)。
的質量為____kg(用含字母的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知H2O2、KMnO4、NaClO、K2Cr2O7均具有強氧化性,將溶液中的Cu2+、Fe2+、Fe3+沉淀為氫氧化物,需溶液的pH分別為6.4、6.4、3.7。現有含FeClx雜質的氯化銅晶體(CuCl2·2H2O),為制取純凈的CuCl2·2H2O,首先將其制成水溶液,然后按圖示步驟進行提純:

請回答下列問題:
(1)本實驗最適合的氧化劑X是__________。(選填下面的序號)
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)物質Y是__________。
(3)本實驗用加堿沉淀的目的是否能達到?__________。原因是__________。
(4)加氧化劑的目的為__________。
(5)最后能不能直接蒸發結晶得到CuCl2·2H2O晶體?________。如何操作?__________。·
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式書寫正確的是
A.銅粉加入氯化鐵溶液中:Cu + Fe3+ = Fe2++Cu2+
B.將稀硫酸滴在銅片上:Cu + 2H+ =Cu2++ H2↑
C.氯氣與燒堿溶液反應:Cl2+2OH-=ClO-+Cl-+H2O
D.將少量銅屑放入稀硝酸中:Cu+4H++2NO![]() = Cu2++2NO2↑+2H2O
= Cu2++2NO2↑+2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】N2(g)與H2(g)在一定條件下經歷如下過程生成NH3(g)。下列說法正確的是

A.I中破壞的均為極性鍵
B.Ⅱ、Ⅲ、Ⅳ均為吸熱過程
C.Ⅳ中NH2與H2生成NH3
D.該條件下生成1molNH3放熱54kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物A可用作果實催熟劑。某同學欲以A為主要原料合成乙酸乙酯,其合成路線如圖所示。
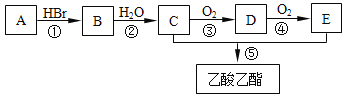
請回答:
(1)C分子中含有的官能團名稱是___________; C的同分異構體的核磁共振氫譜只有一種類型氫原子的吸收峰,其結構簡式是___________。
(2)反應①的反應類型是_________反應,反應 ②~⑤ 中反應類型相同的是_______和_______、_________和________(填序號)。
(3)由A可以直接轉化為C,其反應的化學方程式是___________。
(4)反應②的化學方程式是____________,反應⑤的化學方程式是______。
(5)為了檢驗B中的溴元素,以下操作合理的順序是________(填序號)。
a.加AgNO3 溶液 b.加NaOH 溶液 c.加熱 d.加稀硝酸至溶液顯酸性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求填空:
I.(1)AlCl3的水溶液pH______7(填>、=、<=,其原因為______________(用離子方程式表示),將其溶液加熱蒸干并灼燒最終得到物質是_____________________(填化學式)。
(2)常溫下,Cr(OH)3的溶度積Ksp=c(Cr3+)·c3(OH)=1032,要使c(Cr3+)降至105mol/L,溶液的pH應調至_____________。
(3)物質的量濃度相同的三種溶液:①NH4Cl ②氨水 ③NH4HSO4,c(NH4+)大小順序正確的是______________。(用序號表示)
(4)常溫下兩種溶液:a.pH=4 NH4Cl b.pH=4鹽酸溶液,其中水電離出C(H+)之比為____________________。
II.室溫下,某一元弱酸HA的電離常數K=1.6×10-6。 向20.00 mL 濃度約為0.1 mol·L-1 HA溶液中逐滴加入0.1000 mol·L-1 的標準NaOH溶液,其pH變化曲線如圖所示(忽略溫度變化)。請回答下列有關問題:

(1)a、b、c、d四點中水的電離程度最大的是________點,滴定過程中宜選用________作指示劑,滴定終點在________(填“c點以上”或“c點以下”)。
(2)滴定過程中部分操作如下,下列各操作使測量結果偏高的是___________(填字母序號)。
A.滴定前堿式滴定管未用標準NaOH溶液潤洗
B.用蒸餾水洗凈錐形瓶后,立即裝入HA溶液后進行滴定
C.滴定過程中,溶液出現變色后,立即停止滴定
D.滴定結束后,仰視液面,讀取NaOH溶液體積
(3)若重復三次滴定實驗的數據如下表所示,計算滴定所測HA溶液的物質的量濃度為___mol/L。(保留4位有效數字)
實驗序號 | NaOH溶液體積/mL | 待測HA溶液體積/mL |
1 | 21.01 | 20.00 |
2 | 20.99 | 20.00 |
3 | 21.60 | 20.00 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com