
分析 (1)二氧化硫與氧化鈣反應生成亞硫酸鈣,亞硫酸鈣與氧氣反應生成硫酸鈣;
(2)①二氧化硫與碳酸鈣、氧氣反應生成硫酸鈣、二氧化碳;
②二氧化硫與氫氧化鈣、氧氣反應生成硫酸鈣和水;
氫氧化鈣的溶解度較小,吸收SO2的量少.
解答 解:(1)二氧化硫與氧化鈣反應生成亞硫酸鈣方程式:CaO+SO2=CaSO3,亞硫酸鈣與氧氣反應生成硫酸鈣:2CaSO3+O2=2CaSO4;
故答案為:CaO+SO2=CaSO3;2CaSO3+O2=2CaSO4;
(2)①二氧化硫與碳酸鈣、氧氣反應生成硫酸鈣、二氧化碳,方程式:2SO2+O2+2CaCO3═2CaSO4+2CO2;
故答案為:2SO2+O2+2CaCO3═2CaSO4+2CO2;
②二氧化硫與氫氧化鈣、氧氣反應生成硫酸鈣和水,化學方程式:2SO2+O2+2Ca(OH)2=2CaSO4+2H2O;
故答案為:2SO2+O2+2Ca(OH)2=2CaSO4+2H2O;
因為氫氧化鈣的溶解度較小,得到的澄清石灰水的濃度較小,吸收SO2的量少,所以熟石灰懸濁液吸收SO2速度快且脫硫率高.熟石灰固體與氣體接觸面小吸收速度慢且脫硫率低,所以不用澄清石灰水或熟石灰的固體吸收二氧化硫,
故答案為:熟石灰懸濁液吸收SO2速度快且脫硫率高.澄清石灰水中Ca(OH)2濃度較小,吸收SO2的量少;熟石灰固體與氣體接觸面小吸收速度慢且脫硫率低.
點評 本題考查了工業脫硫的原理,側重化學方程式的書寫,明確二氧化硫的還原性是解題關鍵,為高考頻考題,注意對相關知識的積累,題目難度不大.


 天天練口算系列答案
天天練口算系列答案科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,Na2O2與足量H2O反應,共生成0.2molO2,轉移電子的數目為0.8NA | |
| B. | 25℃,pH=13的NaOH溶液中含有OH-的數目為0.1NA | |
| C. | 1mol甲基(-14C1H3)所含的中子數和電子數分別為8NA、9NA | |
| D. | 含4molHCl的濃鹽酸與足量的二氧化錳在加熱條件下反應,一定能產生NA個Cl2氣體分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | A | B | C | D |
| 實驗 | 除去氯化鈉晶體中混有的氯化銨晶體 | 分離CCl4中的I2 | 分離酒精和水 | 除去CO氣體中的CO2氣體 |
| 裝置 | 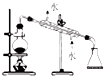 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{24}^{52}$Cr | B. | ${\;}_{12}^{24}$Mg | C. | ${\;}_{26}^{56}$Fe | D. | ${\;}_{22}^{48}$Ti |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向NaAlO2溶液中通入過量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| B. | 少量SO2通入苯酚鈉溶液中:C6H5O-+SO2+H2O═C6H5OH+HSO3- | |
| C. | 向海帶灰浸出液中加入稀硫酸、雙氧水:2I-+2H++H2O2═I2+2H2O | |
| D. | 用濃鹽酸酸化的KMnO4溶液與H2O2反應,證明H2O2具有還原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  用于證明非金屬性強弱:Cl>C>Si | B. |  用于分離I2和NH4Cl | ||
| C. |  裝置能組成Zn、Cu原電池 | D. |  用于測定某稀鹽酸的物質的量濃度 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com