
| A. | 電解時,鐵棒連接電源的負極 | |
| B. | 鐵棒的電極反應式為Fe+6e-+8OH-═FeO42-+4H2O | |
| C. | 若Ⅲ區生成1mol Na2FeO4,Ⅰ區將生成67.2L H2 | |
| D. | 電解總反應的離子方程式為Fe+2OH-+2H2O$\frac{\underline{\;電解\;}}{\;}$FeO42-+3H2↑ |
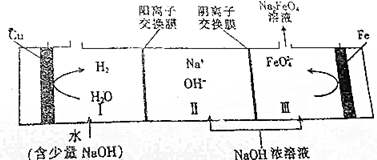
分析 由工作原理示意圖可知,鐵失電子生成高鐵酸鈉,水獲得電子生成氫氣,則鐵作陽極,Cu作陰極,陽極電極方程式為:Fe-6e-+8OH-═FeO42-+4H2O,陰極電極方程式為2H++2e-=H2↑或2H2O+2e-=H2↑+2OH-,Ⅱ室中鈉離子經過陽離子交換膜進入I室,Ⅱ室中OH-離子經過陰離子交換膜進入Ⅲ室.
解答 解:A.由工作原理示意圖可知,鐵失電子生成高鐵酸鈉,水獲得電子生成氫氣,則鐵作陽極,Cu作陰極,電解時,鐵棒連接電源的正極,故A錯誤;
B.陽極是鐵失電子生成高鐵酸鈉,陽極電極方程式為:Fe-6e-+8OH-═FeO42-+4H2O,故B正確;
C.陽極電極方程式為:Fe-6e-+8OH-═FeO42-+4H2O,若Ⅲ區生成1mol Na2FeO4,則轉移電子為6mol,陰極電極方程式為2H++2e-=H2↑或2H2O+2e-=H2↑+2OH-,可知陰極生成氫氣為3mol,但氫氣不一定是標況下,故氫氣體積不一定是67.2L,故C錯誤;
D.電解總反應的離子方程式為:Fe+2OH-+2H2O$\frac{\underline{\;電解\;}}{\;}$FeO42-+3H2↑,故D正確,
故選:BD.
點評 本題考查了電解原理,正確判斷陰陽極及發生的反應是解本題關鍵,易錯選項是C,注意氣體摩爾體積的適用范圍和條件.


科目:高中化學 來源: 題型:選擇題
| A. | 32 g O2含有的氧原子數目為2NA | |
| B. | 56 g的Fe在足量Cl2中完全燃燒轉移電子數為2NA | |
| C. | 1 mol•L-1 Na2SO4溶液含有的鈉離子數目為2NA | |
| D. | 標準狀況下,22.4 L苯含有的碳原子數目為6NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Al、Cu、Mg、Ag、Fe | B. | Fe、Cu、Al、Ag、Mg | C. | Mg、Ag、Al、Cu、Fe | D. | Mg、Cu、Al、Ag、Fe |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 8種 | B. | 9種 | C. | 12種 | D. | 13種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
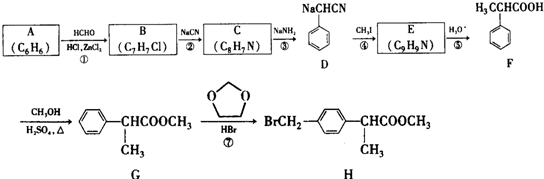
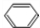 +HCHO+HCl$\stackrel{ZnCl_{2}}{→}$
+HCHO+HCl$\stackrel{ZnCl_{2}}{→}$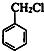 +H2O.
+H2O.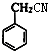 ;E的結構簡式為
;E的結構簡式為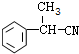 .
. .
.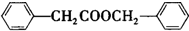 的合成路線
的合成路線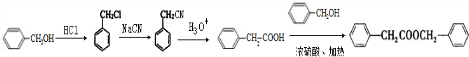 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | W、Y、Z三種元素的最高價氧化物的水化物可能有兩種是強堿、一種是強酸 | |
| B. | Z元素在第三周期第ⅥA族 | |
| C. | W、Y、Z三種元素有兩種是金屬、一種是非金屬 | |
| D. | W、X、Y三種元素的單質熔沸點依次降低 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 中和熱的測定實驗(如圖).
中和熱的測定實驗(如圖).查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的電離程度前者比后者大 | |
| B. | 反應Hg(1)+H2SO4(aq)=HgSO4(aq)+H2(g)在常溫下不能自發進行,則△H>0 | |
| C. | 將純水加熱至較高溫度,K變大、pH變小、呈酸性 | |
| D. | N2(g)+3H2(g)?2NH3(g)△H<0,其他條件不變時增大氮氣的濃度,正逆反應速率均增大,平衡正向移動,氫氣的轉化率提高 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com