
| A. | C02分子中σ鍵和π鍵之比為1:1 | |
| B. | PCl5中所有原子均滿足8電子穩定結構 | |
| C. | 由于HCOOH分子間存在氫鍵,則同壓下,HC00H的沸點比CH3OCH3的高 | |
| D. | CH2=CH-CHO分子中碳原子的雜化類型均為sp2 |
分析 A.共價單鍵為σ鍵,共價雙鍵中含有一個σ鍵、一個π鍵,二氧化碳結構式為O=C=O;
B.在共價化合物中,中心原子最外層電子數+化合價的絕對值=8,則該分子中所有原子都達到8電子穩定結構,但氫化物除外;
C.分子晶體中,含有氫鍵的物質熔沸點較高;
D.丙烯醛中所有C原子價層電子對個數都是3,根據價層電子對互斥理論判斷雜化類型.
解答 解:A.共價單鍵為σ鍵,共價雙鍵中含有一個σ鍵、一個π鍵,二氧化碳結構式為O=C=O,所以二氧化碳分子中含有一個σ鍵、一個π鍵,則σ鍵和π鍵之比為1:1,故A正確;
B.在共價化合物中,中心原子最外層電子數+化合價的絕對值=8,則該分子中所有原子都達到8電子穩定結構,但氫化物除外,該物質中P原子最外層電子式+化合價的絕對值=5+5=10,所以該分子中P原子不滿足8電子穩定結構,故B錯誤;
C.分子晶體中,含有氫鍵的物質熔沸點較高,甲酸中含有氫鍵、甲醚中不含氫鍵,所以甲酸熔沸點高于甲醚,故C正確;
D.丙烯醛中所有C原子價層電子對個數都是3,根據價層電子對互斥理論知,該分子中3個C原子都采用sp2雜化,故D正確;
故選B.
點評 本題考查原子雜化方式判斷、氫鍵、物質結構等知識點,明確物質結構、氫鍵對物質性質影響及價層電子對互斥理論即可解答,這些都是高頻考點,注意:氫鍵只影響物理性質不影響化學性質,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 檢測時,電解質溶液中的H+向負極移動 | |
| B. | 若有 0.4 mol電子轉移,則在標準狀況下消耗 4.48 L氧氣 | |
| C. | 電池反應的化學方程式為:CH3CH2OH+O2═CH3COOH+H2O | |
| D. | 正極上發生的反應為:O2+4e-+2H2O═4OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO3 | B. | NO2 | C. | Si | D. | CH3COOH |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
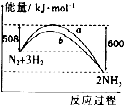
| A. | 加人催化劑后,反應過程的能量變化可用曲線b表示 | |
| B. | 生成物的總能量小于反應物的總能量 | |
| C. | 熱化學方程式為:N2(g)+3H2(g)?2NH3(g)△H=-92 kJ•mol-1 | |
| D. | 在298 K、恒容密閉容器中,通人1 mol N2和3 mol H,充分反應后放出的熱量為92kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①⑤⑥ | B. | ②③④⑤ | C. | ①③④⑥ | D. | ②③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分子晶體中一定存在分子間作用力,不一定有共價鍵 | |
| B. | 元素的非金屬性越強,其單質的活潑性越強 | |
| C. | 含有金屬陽離子的晶體不一定是離子晶體,離子晶體中一定含金屬陽離子 | |
| D. | 溶于水后可電離出能自由移動離子的晶體一定是離子晶體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加熱 | |
| B. | 加入少量CuSO4溶液 | |
| C. | 不用稀硫酸,改用質量分數為98%的濃硫酸 | |
| D. | 不用鐵片,改用鐵粉 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗序號 | 加入試劑 | 實驗現象 |
| Ⅰ | 4mL 2mol/L NH4Cl 溶液 | 沉淀溶解 |
| Ⅱ | 4mL蒸餾水 | 沉淀不溶解 |
| 序號 | 實驗內容 | 結 果 |
| 1 | 測定醋酸銨溶液的pH | pH約為7,溶液呈中性 |
| 2 | 取少量的相同質量的氫氧化鎂分別盛放在試管中,分別向其中滴加醋酸銨溶液和氯化銨溶液 | 固體均溶解 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 提倡騎自行車或乘公交車上下班 | B. | 提倡使用一次性木筷 | ||
| C. | 推廣使用無磷洗衣粉和無氟冰箱 | D. | 將煤液化或氣化,獲得清潔燃料 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com