
已知:將Cl2通人適量KOH溶液,產物中可能有KC1、KClO、KC1O3,且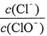 的值與溫度高低有關。當n(KOH)=amol時,下列有關說法錯誤的是
的值與溫度高低有關。當n(KOH)=amol時,下列有關說法錯誤的是
A.若某溫度下,反應后 =11,則溶液中
=11,則溶液中 =
=
參加反應的氯氣的物質的量等于 amol
amol
C.改變溫度,反應中轉移電子的物質的量ne的范圍: amol≤ne≤
amol≤ne≤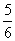 amol
amol
D.改變溫度,產物中KC1O3的最大理論產量為 amol
amol
科目:高中化學 來源: 題型:
現有五種可溶性物質A、B、C、D、E,它們所含的陰、陽離子互不相同,分別含有五種陽離子K+、Fe3+、Cu2+、Ba2+、Al3+和五種陰離子Cl-、OH-、NO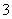 、CO
、CO 、X中的一種。
、X中的一種。
(1)某同學通過比較分析,認為無須檢驗就可判斷其中必有的兩種物質是________和________。
(2)物質C中含有離子X。為了確定X,現將(1)中的兩種物質記為A和B,當C與A的溶液混合時產生藍色沉淀,向該沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固體,則X為________(填字母)。
A.Br- B.SO
C.CH3COO-  D.HCO
D.HCO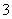
(3)將19.2 g Cu投入裝有足量D溶液的試管中,Cu不溶解,再滴加稀H2SO4,Cu逐漸溶解,管口附近有紅棕色氣體出現,寫出Cu溶解的離子方程式__________________,若要將Cu完全溶解,至少加入H2SO4的物質的量是____________________。
Cu投入裝有足量D溶液的試管中,Cu不溶解,再滴加稀H2SO4,Cu逐漸溶解,管口附近有紅棕色氣體出現,寫出Cu溶解的離子方程式__________________,若要將Cu完全溶解,至少加入H2SO4的物質的量是____________________。
(4)E溶液與氫碘酸反應時可生成棕色物質,該反應的離子方程式為_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
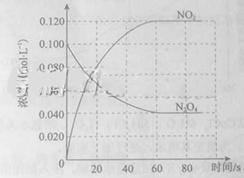
在容積為1.00L的容器中,通入一定量的N2O4,發生反應N2O4(g) 2NO2(g),隨溫度升高,混合氣體的顏色變深。
2NO2(g),隨溫度升高,混合氣體的顏色變深。
回答下列問題:
(1)反應的△H 0(填“大于”“小于”);100℃時,體系中各物質濃度隨時間變化如上圖所示。在0~60s時段,反應速率v(N2O4)為 mol·L-1·s-1反應的平衡常數K1為 。
(2)100℃時達到平衡后,改變反應溫度為T,c(N2O4)以0.0020 mol·L-1·s-1的平均速率降低,經10s又達到平衡。
①T 100℃(填“大于”“小于”),判斷理由是 。
②列式計算溫度T是反應的平衡常數K2
(3)溫度T時反應達平衡后,將反應容器的容積減少一半,平衡向 (填“正反應”或“逆反應”)方向移動,判斷理由是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
在10L恒容密閉容器中充入X(g)和Y(g),發生反應X(g)+Y(g) M(g)+N(g),所得實驗數據如下表:
M(g)+N(g),所得實驗數據如下表:
| 實驗 編號 | 溫度/℃ | 起始時物質的量/mol | 平衡時物質的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| ④ | 900 | 0.10 | 0.15 | b |
下列說法正確的是
A.實驗①中,若5min時測得n(M)=0.050mol,則0至5min時間內,用N表示的平均反應速率υ(N)=1.0×10-2mol/(L·min)
B.實驗②中,該反應的平衡常數K=2.0
C.實驗③中,達到平衡是,X的轉化率為60%
D.實驗④中,達到平衡時,b>0.060
查看答案和解析>>
科目:高中化學 來源: 題型:
下列敘述錯誤的是
A. SO2使溴水褪色與乙烯使KMnO4溶液褪色的原理相同
B.制備乙酸乙酯時可用熱的NaOH溶液收集產物以除去其中的乙酸
C.用飽和食鹽水替代水跟電石反應,可以減緩乙炔的產生速率
D.用AgNO3溶液可以鑒別KC1和KI
查看答案和解析>>
科目:高中化學 來源: 題型:
NH3經一系列反應可以得到HNO3,如下圖所示。
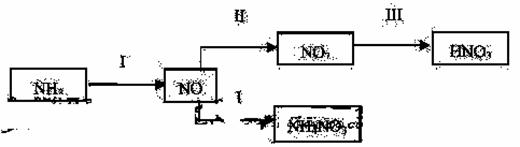
 (1)I中,NH3 和O2在催化劑作用下反應,其化學方程式是_____________________。
(1)I中,NH3 和O2在催化劑作用下反應,其化學方程式是_____________________。
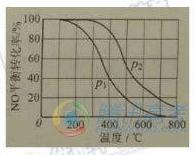
(2)II中,2NO(g)+O2 2NO2(g)。在其他條件相同時,分別測得NO的平衡轉化率在不同壓強(P1、P2)下溫度變化的曲線(如右圖)。
2NO2(g)。在其他條件相同時,分別測得NO的平衡轉化率在不同壓強(P1、P2)下溫度變化的曲線(如右圖)。
①比較P1、P2的大小關系:________________。
②隨溫度升高,該反應平衡常數變化的趨勢是________________。
(3)III中,將NO2(g)轉化為N2O4(l),再制備濃硝酸。
①已知:2NO2(g) N2O4(g)△H1
N2O4(g)△H1
2NO2(g) N2O4(l)△H2
N2O4(l)△H2
下列能量變化示意圖中,正確的是(選填字母)_______________。
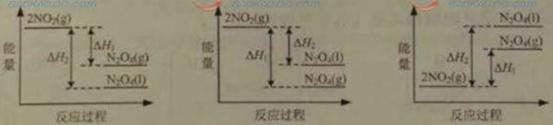
A B C
②N2O4與O2、H2O化合的化學方程式是_________________。
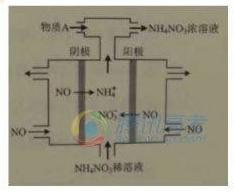
(4)IV中,電解NO制備 NH4NO3,其工作原理如右圖所示,為使電解產物全部轉化為NH4NO3,需補充物質A,A是_____________,說明理由:________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
某化學興趣小組為探究元素性質的遞變規律,設計了如下系列實驗。
Ⅰ.(1)將鈉、鉀、鎂、鋁各1 mol分別投入到足量的0.1 mol·L-1的鹽酸中,試預測實驗結果:________________________________________________________________________
與鹽酸反應最劇烈,___________ _______與鹽酸反應最慢。
_______與鹽酸反應最慢。
(2)將NaOH溶液與NH4Cl溶液混合生成NH3·H2O,從而驗證NaOH的堿性大于NH3·H2O,繼而可以驗證Na的金屬性大于N,你認為此設計是否合理?并說明理由:________________________________________________________________________
________________________________________________________________________。
Ⅱ.利用下圖裝置可以驗證非金屬性的變化規律。
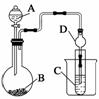
(3)儀器A的名稱為________,干燥管D的作用是____________________________。
(4)實驗室中現有藥品Na2S、KMnO4、濃鹽酸、MnO2,請選擇合適藥品設計實驗驗證氯的非金屬性大于硫:裝置A、B、C中所裝藥品分別為________、________、________,裝置C中的實驗現象為有淡黃色沉淀生成,離子方程式為________________________________________________________________________。
(5)若要證明非金屬性:C>Si,則A中加________、B中加Na2CO3、C中加________,觀察到C中溶液的現象為________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
下列變化為放熱反應的是( )
A.H2O(氣)=H2O(液)
B.Ba(OH)2·8H2O晶體與NH4Cl晶體混合并攪拌
C.形成化學鍵時共放出能量862kJ的化學反應
D.能量變化如下右圖所示的化學反應
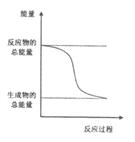
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com