
 研究NO2、SO2、CO等大氣污染氣體的處理具有重要意義.
研究NO2、SO2、CO等大氣污染氣體的處理具有重要意義.分析 (1)反應中NO2中N元素化合價由+4降低為氮氣中0價,據此計算NO2的物質的量,再根據V=nVm計算NO2的體積;
(2)根據蓋斯定律計算反應熱;
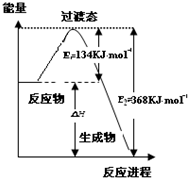
(3)加入催化劑能降低反應所需的活化能,但是不改變反應物的總能量和生成物的總能量,由圖可知,1mol NO2和1mol CO反應生成CO2和NO放出熱量368-134=234kJ,根據熱化學方程式書寫原則進行書寫;
(4)該燃料電池中,負極上CO失電子和碳酸根離子反應生成二氧化碳,正極上氧氣得電子和二氧化碳反應生成碳酸根離子,根據電解食鹽水的總反應來及計算回答,據此分析解答.
解答 解:(1)反應中NO2中N元素化合價由+4降低為氮氣中0價,轉移1.2mol電子時,消耗的NO2的物質的量=$\frac{1.2mol}{4}$=0.3mol,故消耗NO2的體積=0.3mol×22.4L/mol=6.72L,故答案為:6.72;
(2)已知:①2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ•mol-1
②2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ•mol-1
根據蓋斯定律,(①-②)×$\frac{1}{2}$得:NO2(g)+SO2(g)?SO3(g)+NO(g) 故△H=$\frac{1}{2}$×[(-196.6kJ•mol-1)-(-113.0kJ•mol-1)]=-41.8kJ•mol-1,故答案為:-41.8;
(3)加入催化劑能降低反應所需的活化能,則E1和E2都減小,催化劑不能改變反應物的總能量和生成物的總能量之差,即反應熱不改變,所以催化劑對反應熱無影響,由圖可知,1mol NO2和1mol CO反應生成CO2和NO放出熱量368-134=234kJ,反應熱化學方程式為NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1,
故答案為:減小;不變;NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1;
(4)該熔融鹽燃料電池中,正極上氧氣得電子和二氧化碳反應生成碳酸根離子,電極反應式為O2+2CO2+4e-═2 CO32-,負極上燃料CO失電子和碳酸根離子反應生成二氧化碳,電極反應式為2CO+2CO32--4e-═4CO2;電解氯化鈉溶液反應的離子方程式為:2Cl-+2H2O$\frac{\underline{\;通電\;}}{\;}$2OH-+H2↑+Cl2↑,根據總反應當兩極上共收集到0.448L即0.02 mol氣體時,則生成的氯氣和氫氣均是0.01mol,所以生成氫氧化鈉的物質的量是0.02mol,所以氫氧化鈉的濃度C=$\frac{n}{V}$=V$\frac{0.02mol}{0.2L}$=0.1mol/L,所以pH=13,
故答案為:CO-2e-+CO32-=2CO2; 2Cl-+2H2O═Cl2↑+H2↑+2OH-;13.
點評 本題考查較為綜合,題目難度中等,涉及氧化還原反應計算、電化學知識、反應熱計算、注意熱化學方程式的書寫方法和計算應用,注意焓變計算和物質聚集狀態的標注,學習中要準確把握.


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化學 來源: 題型:選擇題
| A. | 為了防止蛋白質鹽析,疫苗等生物制劑應冷凍保藏 | |
| B. | 污水處理可采用混凝法,明礬是一種常用的混凝劑 | |
| C. | 硅單質常作為制備光導纖維的主要材料 | |
| D. | 淘米水中含有淀粉可以直接檢測加碘鹽中是否含有碘元素 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 蒸發 | B. | 過濾 | C. | 萃取 | D. | 蒸餾 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
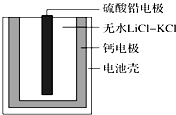 熱激活電池可用作火箭、導彈的工作電源.一種熱激活電池的基本結構如圖所示,其中作為電解質的無水LiCl-KCl混合物受熱熔融后,電池即可瞬間輸出電能.該電池總反應為PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有關說法正確的是( )
熱激活電池可用作火箭、導彈的工作電源.一種熱激活電池的基本結構如圖所示,其中作為電解質的無水LiCl-KCl混合物受熱熔融后,電池即可瞬間輸出電能.該電池總反應為PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有關說法正確的是( )| A. | 正極反應式:Ca+2Cl--2e-=CaCl2 | |
| B. | 放電過程中,Li+向負極移動 | |
| C. | 常溫時,在正負極間接上電流表或檢流計,指針發生偏轉 | |
| D. | 每轉移0.1 mol電子,理論上生成10.35g Pb |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
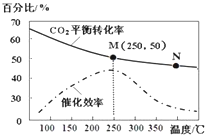
| A. | 生成乙烯的速率:v(M)一定小于v(N) | |
| B. | 化學平衡常數:KN>KM | |
| C. | 當溫度高于250℃時,升高溫度,平衡向逆反應方向移動,從而使催化劑的催化效率降低 | |
| D. | 若投料比n(H2):n(CO2)=3:1,則圖中M點時,乙烯的體積分數為7.7% |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
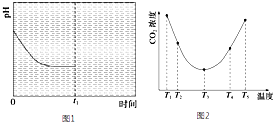 減少二氧化碳的排放以及資源化利用具有重要意義.
減少二氧化碳的排放以及資源化利用具有重要意義.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該電池的正極為鋅 | |
| B. | 該電池反應中二氧化錳起催化劑作用 | |
| C. | 當 0.lmol Zn 完全溶解時,流經電解液的電子個數為 1.204×l023 | |
| D. | 電池正極反應式為:2MnO2+2e一+2H2O═2MnO (OH)+2OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
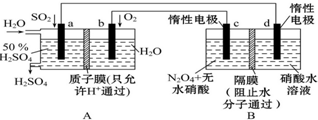 膜技術原理在化工生產中有著廣泛的應用.有人設想利用電化學原理制備少量硫酸和綠色硝化劑N2O5(N2O5極易和水反應),裝置如圖:
膜技術原理在化工生產中有著廣泛的應用.有人設想利用電化學原理制備少量硫酸和綠色硝化劑N2O5(N2O5極易和水反應),裝置如圖:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com