
| A. | pH=4的NaHSO3溶液中:c(Na+)>c(H+)>c(HSO3-)>c(SO32-)>C(OH-) | |
| B. | 0.2mol•L-1Na2CO3溶液和0.1mol•L-1鹽酸等體積混合,在混合溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| C. | 等體積、等濃度的HR溶液和NaOH溶液混合,溶液中一定存在:c(Na+)>c(R-)>c(OH-)>c(H+) | |
| D. | 等體積、等濃度的①CH3COONa②NaNO3③NaClO溶液中離子總數:②>①>③ |
分析 A.pH=4的NaHSO3溶液中,溶液顯酸性,溶液中HSO3-電離大于水解;
B.0.2mol•L-1Na2CO3溶液和0.1mol•L-1鹽酸等體積混合,得到等濃度的NaHCO3和Na2CO3,溶液中碳酸根離子水解程度大于碳酸氫根離子溶液顯堿性;
C.等體積、等濃度的HR溶液和NaOH溶液混合,若HR為強酸c(OH-)=c(H+),若HR為弱酸,反應后溶液中c(OH-)>c(H+);
D.等體積、等濃度的①CH3COONa溶液中醋酸根離子水解溶液顯堿性,②NaNO3 溶液中離子不水解,溶液呈中性,③NaClO溶液中次氯酸根離子水解溶液顯堿性,醋酸根離子水解程度小于次氯酸根離子水解程度,結合溶液電荷守恒比較;
解答 解:A.pH=4的NaHSO3溶液顯酸性,溶液中離子濃度大小為:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>C(OH-),故A錯誤;
B.0.2mol•L-1Na2CO3溶液和0.1mol•L-1鹽酸等體積混合,得到等濃度的NaHCO3和Na2CO3,溶液中碳酸根離子水解程度大于碳酸氫根離子溶液顯堿性,溶液中c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),故B錯誤;
C.等體積、等濃度的HR溶液和NaOH溶液混合,若HR為強酸c(OH-)=c(H+),若HR為弱酸,反應后溶液中c(OH-)>c(H+),離子濃度大小不一定,故C錯誤;
D.等體積、等濃度的①CH3COONa②NaNO3③NaClO溶液中存在電荷守恒,①c(H+)+c(Na+)=c(OH-)+c(CH3COO-),②溶液中電荷守恒c(H+)+c(Na+)=c(OH-)+c(NO3-)③溶液中電荷守恒c(H+)+c(Na+)=c(ClO-)+c(OH-),硝酸鈉溶液中無離子水解,離子水解離子減小,溶液中醋酸根離子水解程度小于次氯酸根離子,所以離子總數:②>①>③,故D正確;
故選D.
點評 本題考查了電解質溶液中離子濃度大小比較,酸堿反應后溶液酸堿性的定量分析判斷,電解質溶液中鹽類水解、弱電解質電離和溶液中電荷守恒的理解應用,題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一定濃度的醋酸鈉溶液可使酚酞溶液變紅,其原因是發生了如下反應:CH3COO-+H2O?CH3COOH+OH-,使得溶液中的c(OH-)>c(H+) | |
| B. | 在常溫下,10 mL 0.2 mol•L-1鹽酸與10 mL 0.2 mol•L-1 Ba(OH)2溶液充分混合,若混合后溶液的體積為20 mL,則溶液的pH=13 | |
| C. | 在0.1 mol•L-1 NH4Cl溶液中:c(H+)+c(NH4+=c(Cl-) | |
| D. | 5 mL 1 mol•L-1 CH3COONa溶液與5 mL 1 mol•L-1鹽酸混合液中c(Cl-)=c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
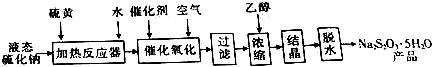
| 溶液溫度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 氧化完全所需時間/h | 6 | 5.5 | 5.5 | 6 | 20 | 16 | 11 | 11 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 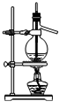 石油的分餾 | B. | 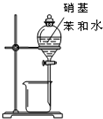 分離硝基苯和水 | ||
| C. | 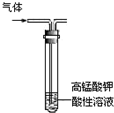 除去甲烷中的乙烯 | D. | 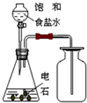 制取并收集乙炔氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 硫酸與氫氧化鋇在溶液中反應Ba2++SO42-═BaSO4↓ | |
| B. | 氫氧化鎂溶于稀硫酸:2H++Mg(OH)2═Mg2++2H2O | |
| C. | 大理石與鹽酸反應 CO32-+2H+═H2O+CO2↑ | |
| D. | 少量金屬鈉投入到CuSO4溶液中 2Na+Cu2+═2Na++Cu |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K+、Ca2+、Cl-、SO42- | B. | NH4+、HCO3-、Cl-、K+ | ||
| C. | Cl-、Na+、NO3-、Ca2+ | D. | MnO4-、NO3-、Na+、Cl- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com