
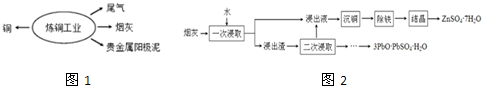
分析 流程圖2整體分析如下:煙灰加入水,浸出液中含Cu2+,加入鋅粉(或鐵粉),置換出銅(沉銅),溶液中為ZnSO4、FeSO4再加入堿使鐵元素沉淀并分離出去(除鐵),結晶可得到ZnSO4.7H2O,
(1)根據物質的性質,分析可發生反應的物質和產品之間的關系,寫出相關反應;
(2)①根據流程圖,分析“沉銅”前后,銅元素發生的變化,找出恰當的物質;
②根據銅的化合物的溶解性回答;
(3)根據“陽氧陰還”,陰極發生還原反應,得電子,再結合離子放電順序,即可得出答案;再抓住題給信息“產生的氣體遇空氣迅速變為紅棕色”,利用守恒關系解答.
解答 解:(1)氨水中主要成分為NH3.H2O,可與酸性氧化物SO2反應生成鹽與水,方程式為:SO2+2NH3.H2O=(NH4)2SO3+H2O,再加入硫酸,發生復分解反應:鹽+較強酸=另一種鹽+較弱的酸,方程式如下:(NH4)2SO3+H2SO4=H2O+SO2↑+(NH4)2SO4
故答案為:SO2+2NH3.H2O=(NH4)2SO3+H2O;(NH4)2SO3+H2SO4=H2O+SO2↑+(NH4)2SO4;
(2)①通過流程圖可以看出,浸出液中含有能溶于水的Cu2+,沉銅則需要將其轉化為單質銅,所以需要加入還原性比銅強的金屬,考慮不引入其他雜質,最好加入鋅粉(鐵粉也可以),
故答案為:鋅粉(或鐵粉);
②根據流程圖2看出,第一次用水浸取,可浸出能溶于水的化合物,不溶于水的CuO則在浸出渣中,所以要提高浸出率,應選能溶解CuO的酸,結合流程圖,選用的是硫酸,
故答案為:CuO;H2SO4;
(3)陰極得電子,發生還原反應,所以為:Ag++e-=Ag;根據題目信息“產生的氣體遇空氣迅速變為紅棕色”,可推測是“NO遇空氣中的O2生成NO2”的現象,所以產生的氣體是NO,再根據原子守恒,電荷守恒,寫出反應為:NO3-+4H++3e-=NO↑+2H2O,
故答案為:Ag++e-=Ag;NO3-+4H++3e-=NO↑+2H2O.
點評 此類題目,一定要理解題意,抓住“暗含”信息,結合化學原理解答,較為簡單,但必須要細心.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 非金屬原子間以共價鍵結合的物質都是共價化合物 | |
| B. | 非極性共價鍵只能存在于非金屬單質中,不可能存在于化合物中 | |
| C. | 含有離子鍵的化合物一定是離子化合物,在離子化合物中可以含有非極性共價鍵 | |
| D. | 凡是能電離出離子的化合物都是離子化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 綠色植物光合作用過程中是由太陽能轉變成化學能 | |
| B. | 研制乙醇汽油技術,可降低機動車輛尾氣中有害氣體的排放 | |
| C. | 煤、石油、天然氣屬于可再生能源 | |
| D. | 利用太陽能等清潔能源代替化石燃料,有利于節約資源、保護環境 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③⑥ | B. | ③④⑤⑥ | C. | ①②③⑥ | D. | ③⑤⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氣體CO2(HCl):通過飽和NaHCO3溶液 | B. | 固體Na2CO3(NaHCO3):加熱 | ||
| C. | 氣體Cl2(HCl):通過NaOH溶液 | D. | FeCl3溶液(FeCl2):通入Cl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
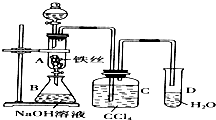 某化學課外小組用右圖裝置制取溴苯.先向分液漏斗中加入苯和液溴,再將混合液慢慢滴入反應器A中(A下端活塞關閉).(已知此反應屬于放熱反應;苯和液溴都易揮發)
某化學課外小組用右圖裝置制取溴苯.先向分液漏斗中加入苯和液溴,再將混合液慢慢滴入反應器A中(A下端活塞關閉).(已知此反應屬于放熱反應;苯和液溴都易揮發)查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com