
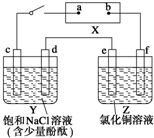
 如圖中X是直流電源.Y槽中c、d為石墨棒,Z槽中e、f是質量相同的銅棒.接通電路后,發現d附近顯紅色.
如圖中X是直流電源.Y槽中c、d為石墨棒,Z槽中e、f是質量相同的銅棒.接通電路后,發現d附近顯紅色.分析 X為直流電源,Y槽中c、d為石墨棒,Z槽中e、f是質量相同的銅棒,接通電路后發現d附近顯紅色,則d附近生成氫氧根離子,則d極為電解池陰極,d電極上氫離子放電生成氫氣和氫氧根離子,c為陽極,c電極上氯離子放電,則a是直流電源正極,b是直流電源負極;電子從原電池的負極流向電解池的陰極,再到陽極,最后流入原電池的正極;結合電解池中兩極上的反應分析
解答 解:X為直流電源,Y槽中c、d為石墨棒,Z槽中e、f是質量相同的銅棒,接通電路后發現d附近顯紅色,則d附近生成氫氧根離子,則d極為電解池陰極,d電極上氫離子放電生成氫氣和氫氧根離子,c為陽極,c電極上氯離子放電,則a是直流電源正極,b是直流電源負極
(1)①由以上分析可知b為負極,故答案為:負;
②Z槽中e與原電池正極相連為陽極;故答案為:陽;
③連接Y、Z槽線路中,電子流動的方向是從e流向d,故答案為:←;
(2)①c為陽極,c電極上氯離子放電,c極上反應的電極反應式為:2Cl--2e-=Cl2↑,故答案為:2Cl--2e-=Cl2↑;
②Y槽中為惰性電極電解氯化鈉溶液,其總反應的化學方程式為2NaCl+2H2O$\frac{\underline{\;通電\;}}{\;}$2NaOH+H2↑+Cl2↑,
故答案為:2NaCl+2H2O$\frac{\underline{\;通電\;}}{\;}$2NaOH+H2↑+Cl2↑;
③Z槽中e極與電源正極相連為陽極,其電極反應式為Cu-2e-═Cu2+,故答案為:Cu-2e-═Cu2+.
(3)①設電路中轉移的電子為xmol,根據e極:Cu-2e-=Cu2+,△m=64 得e極質量減輕:32x(g);
f極:Cu2++2e-=Cu,△m=64 得f極質量增重:32x(g),所以有:32x+32x=2.56,得x=0.04mol,
故答案為:0.04;
②因為兩槽是串聯,電極上流過的電量相等,在電解氯化鈉溶液中,每流過1mol電子,溶液中就會產生1mol氫氧根離子,根據①可知,2min流過0.04mol電子,所以每分鐘溶液中產生的氫氧根的物質的量為0.02mol,所以槽中電解反應的速率v(OH-)=$\frac{\frac{0.02mol}{0.1L}}{1min}$0.2mol/(L•min),故答案為:0.2 mol•L-1•min-1.
點評 本題考查學生電解池的工作原理知識,明確圖中電源的正負極確定以及電解池的陰陽極上的反應是解答的關鍵,并熟悉電極反應及離子的放電順序來解答,題目難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 氧元素和鹵族元素都能形成多種物質,我們可以利用所學物質結構與性質的相關知識去認識和理解.
氧元素和鹵族元素都能形成多種物質,我們可以利用所學物質結構與性質的相關知識去認識和理解.| 氟 | 氯 | 溴 | 碘 | |
(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
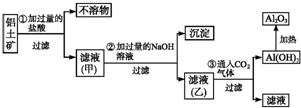 工業上用鋁土礦(主要成分SiO2、Al2O3、Fe3O4)提取氧化鋁作冶煉鋁的原料,提取的操作過程如圖所示:
工業上用鋁土礦(主要成分SiO2、Al2O3、Fe3O4)提取氧化鋁作冶煉鋁的原料,提取的操作過程如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向某溶液中加入稀鹽酸,產生無色無味且能使石灰水變渾濁的氣體,該溶液一定含有CO32- | |
| B. | 用潔凈的鉑絲蘸取少量某溶液在無色火焰上灼燒,火焰呈黃色,該溶液一定是鈉鹽溶液 | |
| C. | 向某溶液中加入BaCl2溶液,有沉淀生成,再加入稀鹽酸,沉淀不消失,該溶液一定含有SO42- | |
| D. | 向某溶液中滴加KSCN 溶液,溶液不變色,滴加氯水后溶液顯紅色,該溶液中一定含Fe2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
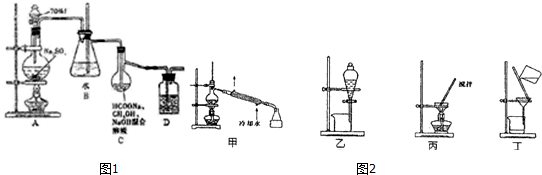
| 乙醇 | 1,2二溴乙烷 | 乙醚 | |
| 狀態 | 無色液體 | 無色液體 | 無色液體 |
| 密度/g/cm2 | 0.79 | 2.2 | 0.71 |
| 沸點/℃ | 78.5 | 132 | 34.6 |
| 熔點/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
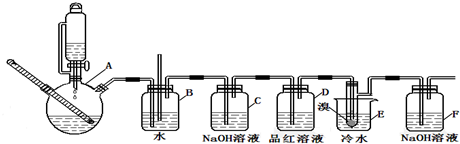
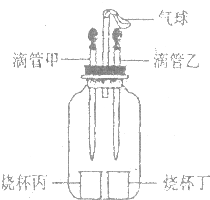 如圖所示裝置(氣密性良好),若先將甲中液體擠出,觀察到氣球明顯鼓起,一段時間后恢復原狀;再將乙中液體擠出,氣球又明顯鼓起.下列組合正確的是( )
如圖所示裝置(氣密性良好),若先將甲中液體擠出,觀察到氣球明顯鼓起,一段時間后恢復原狀;再將乙中液體擠出,氣球又明顯鼓起.下列組合正確的是( )| 選項 | 滴管甲 | 燒杯丙 | 滴管乙 | 燒杯丁 |
| A | 雙氧水 | 二氧化錳 | 水 | 氫氧化鈉 |
| B | 鹽酸 | 鎂 | 鹽酸 | 碳酸納 |
| C | 水 | 氫氧化鈉 | 水 | 硝酸銨 |
| D | 水 | 氧化鈣 | 鹽酸 | 鎂 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙醇和乙酸都是常用調味品的主要成分 | |
| B. | 通過紅外光譜分析可以區分乙醇與乙酸乙酯 | |
| C. | 溴丙烷水解制丙醇與丙烯和水反應制丙醇屬于不同反應類型 | |
| D. | 乙醇和乙酸之間能發生酯化反應,酯化反應和皂化反應互為逆反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 .
.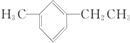 名稱為1-甲基-3-乙基苯.
名稱為1-甲基-3-乙基苯.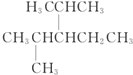 名稱為:2,4-二甲基-3-乙基戊烷.
名稱為:2,4-二甲基-3-乙基戊烷.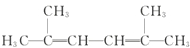 名稱為:2,5-二甲基-2,4-己二烯.
名稱為:2,5-二甲基-2,4-己二烯. ;
;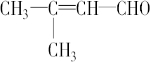 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com