
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 開始沉淀時 | 3.4 | 6.3 | 1.5 |
| 完全沉淀時 | 4.7 | 8.3 | 2.8 |
分析 向鋁灰中加入過量稀H2SO4,A12O3和少量FeO•xFe2O3和硫酸反應生成硫酸鋁、硫酸鐵、硫酸亞鐵,SiO2不反應,過濾除去二氧化硅;向濾液中加入過量KMnO4溶液,高錳酸鉀把亞鐵離子氧化成鐵離子,調節溶液的pH約為3生成氫氧化鐵沉淀,除去鐵離子,過濾,濾液中含鋁離子和過量的高錳酸根離子;加入硫酸錳把過量高錳酸根離子除去,再過濾,對濾液蒸發濃縮、結晶分離出硫酸鋁晶體.
(1)氧化鋁是兩性氧化物溶于強酸強堿;
(2)依據氧化還原反應電子守恒和原子守恒,結合元素化合價變化分析產物和反應物;
(3)依據金屬陽離子沉淀開始和完全沉淀需要的溶液PH分析,亞鐵離子被氧化為鐵離子,調節溶液PH使鐵離子全部沉淀;
(4)①濃鹽酸和二氧化錳再加熱條件下生成黃綠色氣體氯氣;
②加入MnSO4至紫紅色消失,目的是除去過量高錳酸根離子.
解答 解:(1)硫酸溶解氧化鋁生成硫酸鋁和水,反應的離子方程式為:Al2O3+6H+=2Al3++3H2O;
故答案為:Al2O3+6H+=2Al3++3H2O;
(2)反應中MnO4-→Mn2+,Fe2+→Fe3+,MnO4-系數為1,根據電子轉移守恒可知,Fe2+系數為$\frac{7-2}{3-2}$=5,由元素守恒可知,Fe3+系數為5,由電荷守恒可知,由H+參加反應,其系數為8,根據元素原子守恒可知,有H2O生成,其系數為4,方程式配平為MnO4-+5 Fe2++8H+=Mn2++5Fe3++4H2O;
故答案為:MnO4-+5 Fe2++8H+=Mn2++5Fe3++4H2O;
(3)向濾液中加入過量KMnO4溶液,目的是氧化亞鐵離子為三價鐵離子,依據圖表數據分析可知,鐵離子開始沉淀和沉淀完全的溶液PH為1.5--2.8,鋁離子和亞鐵離子開始沉淀的溶液PH大于3,所以調節溶液的pH約為3,可以使鐵離子全部沉淀,鋁離子不沉淀分離;
故答案為:pH約為3時,Fe2+和Al3+不能形成沉淀,將Fe2+氧化為Fe3+,可使鐵完全沉淀;
(4)一定條件下,MnO4-可與Mn2+反應生成MnO2
①向Ⅲ的沉淀中加入濃HCl并加熱,二氧化錳和濃鹽酸在加熱條件下反應生成氯化錳、氯氣和水,生成的氯氣是黃綠色氣體,能說明沉淀中存在MnO2的現象是生成黃綠色氣體;
故答案為:生成黃綠色氣體;
②MnO4-可與Mn2+反應生成MnO2,過濾除去,所以可以利用MnSO4的溶液和高錳酸鉀溶液反應生成二氧化錳,把過量高錳酸根離子除去;
故答案為:除去過量的MnO4-.
點評 本題考查了鎂、鋁、鐵及其化合物性質的應用,主要是混合物分離的方法和實驗設計,加入氧化劑氧化亞鐵離子,調節溶液PH是沉淀分離是解題的關鍵,題目難度中等.


 學而優暑期銜接南京大學出版社系列答案
學而優暑期銜接南京大學出版社系列答案 Happy holiday歡樂假期暑假作業廣東人民出版社系列答案
Happy holiday歡樂假期暑假作業廣東人民出版社系列答案 快樂暑假暑假能力自測中西書局系列答案
快樂暑假暑假能力自測中西書局系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
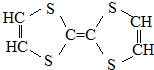
| A. | 它屬于烴的衍生物 | B. | 所有的碳雜化方式相同 | ||
| C. | 屬于高分子化合物 | D. | 它可以與氫氣加成 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 它是高分子化合物 | |
| B. | 它在一定條件下能水解,最終生成葡萄糖 | |
| C. | 是天然蛋白質,僅由C、H、O、N四種元素組成 | |
| D. | 是一種特殊的蛋白質,滴加濃HNO3不發生顏色反應,灼燒時沒有任何氣味 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2-丁烯不存在順反異構體 | |
| B. | 已知丙烷的二氯代物有四種異構體,則其六氯代物的異構體數目為六種 | |
| C. | 菲的結構簡式為 ,它與硝酸反應,可生成4種一硝基取代物 ,它與硝酸反應,可生成4種一硝基取代物 | |
| D. | 乙醇的核磁共振氫譜中有三個峰,峰面積之比是l:2:3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 雷雨時,可增加土壤中硝酸鹽類氮肥的含量 | |
| B. | 許多領域中用液氮制得低溫環境 | |
| C. | 造成光化學煙霧的罪魁禍首是SO2 | |
| D. | 正常雨水因溶有CO2,其pH約為5.6,而酸雨的pH小于5.6 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com