
【題目】如圖是實驗室制氨氣的裝置圖,請回答:
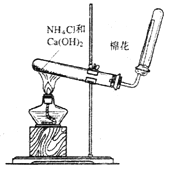
(1)收集氨氣用__法;
(2)實驗室制取氨氣的化學反應方程式:__;
(3)干燥氨氣可選用__;
(4)如何檢驗氨氣是否收集滿:__;
(5)實驗裝置中棉花的作用是:__;
(6)制取出來的氨氣可以遇到一種揮發出來的氣體冒出大量白煙,且產生晶體,寫出化學反應方程式__。
【答案】向下排空氣法 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O 堿石灰 使濕潤的紅色石蕊試紙變藍;也可以用氨氣遇濃鹽酸產生白煙,即“用蘸有濃鹽酸的玻璃棒放在瓶口,產生白煙” 防止氨氣逸出,污染環境 NH3+HCl=NH4Cl
CaCl2+2NH3↑+2H2O 堿石灰 使濕潤的紅色石蕊試紙變藍;也可以用氨氣遇濃鹽酸產生白煙,即“用蘸有濃鹽酸的玻璃棒放在瓶口,產生白煙” 防止氨氣逸出,污染環境 NH3+HCl=NH4Cl
【解析】
結合氨氣的性質,根據實驗室制取氨氣的反應原理、除雜方法、收集方法、驗滿方法等思考。
(1)氨氣易溶于水,且氨氣的密度比空氣的密度小,應用向下排空氣法收集氨氣;
(2)實驗室用氯化銨和堿石灰反應制取氨氣,即堿與鹽反應生成新堿和新鹽,化學方程式為:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
(3)反應過程中會產生水,則氨氣中混有水蒸氣,結合氨氣為堿性氣體,則可用堿石灰吸收水蒸氣,而不能用氯化鈣和無水硫酸銅干燥氨氣;
(4)檢驗氨氣是否集滿,可以利用氨氣的水溶液顯堿性,即用“使濕潤的紅色石蕊試紙變藍”;也可以用氨氣遇濃鹽酸產生白煙,即“用蘸有濃鹽酸的玻璃棒放在瓶口,產生白煙”;
(5)在收集氨氣時氨氣溫度比空氣溫度高,收集的氨氣的濃度小,容易逸出,因此在瓶口塞一團棉花,目的是防止氨氣逸出,污染環境;
(6)NH3和HCl氣體反應生成NH4Cl固體,兩氣體相遇可觀察到大量白煙,發生反應的化學反應方程式為NH3+HCl=NH4Cl。


科目:高中化學 來源: 題型:
【題目】下列各關系式中能說明反應N2+3H2![]() 2NH3已達到平衡狀態的是( )
2NH3已達到平衡狀態的是( )
A. 3v正(N2)=v正(H2) B. v正(N2)=v逆(NH3)
C. 2v正(H2)=3v逆(NH3) D. v正(N2)=3v逆(H2)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應C(s)+H2O(g) ![]() CO(g)+H2(g)在一可變容積的密閉容器中進行,下列條件的改變對其反應速率幾乎無影響的是
CO(g)+H2(g)在一可變容積的密閉容器中進行,下列條件的改變對其反應速率幾乎無影響的是
①增加C的量 ②將容器的體積縮小一半 ③保持體積不變,充入N2使體系壓強增大
④保持壓強不變,充入N2使容器體積增大
A. ①②B. ①③C. ②③D. ③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知下列熱化學方程式:
① H2(g)+1/2O2(g)=H2O(l) ΔH=-285 kJ/mol
② H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8 kJ/mol
③ C(s)+1/2O2(g)=CO(g) ΔH=-241.8 kJ/mol
④ C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol
回答下列各問題:
(1)上述反應中屬于放熱反應的是_______________。
(2)H2的燃燒熱為____________________;C的燃燒熱為__________________。
(3)燃燒10 g H2生成液態水,放出的熱量為___________________。
(4)CO的燃燒熱為_________________;其熱化學方程式為___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關化學反應表達正確的是
A.向CH2BrCOOH中加入足量的氫氧化鈉溶液并加熱:CH2BrCOOH+OH-![]() CH2BrCOO-+H2O
CH2BrCOO-+H2O
B.服用阿司匹林過量出現水楊酸(![]() )中毒反應,可靜脈注射NaHCO3溶液:
)中毒反應,可靜脈注射NaHCO3溶液:![]() + 2 HCO3- →
+ 2 HCO3- →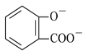 + 2CO2↑ + 2H2O
+ 2CO2↑ + 2H2O
C.乙醛溶液與足量的銀氨溶液共熱:CH3CHO+2[Ag(NH3)2]++2OH-![]() CH3COO-+ NH4++2Ag↓+3NH3↑ +H2O
CH3COO-+ NH4++2Ag↓+3NH3↑ +H2O
D.苯酚鈉溶液中通入少量CO2: CO2+H2O+2C6H5O- → 2C6H5OH+2CO32-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A.已知冰的熔化熱為![]()
![]() ,冰中氫鍵鍵能為20
,冰中氫鍵鍵能為20![]() ,假設1mol冰中有2mol氫鍵,且熔化熱完全用于破壞冰的氫鍵,則最多只能破壞冰中
,假設1mol冰中有2mol氫鍵,且熔化熱完全用于破壞冰的氫鍵,則最多只能破壞冰中![]() 的氫鍵
的氫鍵
B.已知:![]() 石墨
石墨![]() ,
,![]()
![]() .
.![]() ,
,![]()
![]() .
.![]() 石墨
石墨![]() ,
,![]()
![]() .則
.則![]() ,
,![]()
![]()
C.實驗測得環己烷![]() 、環己烯
、環己烯![]() 和苯
和苯![]() 的標準燃燒熱分別為
的標準燃燒熱分別為![]()
![]() 、
、![]()
![]() 和
和![]()
![]() ,可以證明在苯分子中不存在獨立的碳碳雙鍵
,可以證明在苯分子中不存在獨立的碳碳雙鍵
D.已知一定溫度下,醋酸溶液的物質的量濃度為c,電離度為![]() ,
,![]() 若加入少量醋酸鈉固體,則
若加入少量醋酸鈉固體,則![]() 向左移動,
向左移動,![]() 減小,Ka變小
減小,Ka變小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將一定量A、B裝入容積為1 L的恒溫密閉容器中,發生反應:2A(g)+mB(g)![]() nC(g),1 min時達到平衡,C的濃度為x mol·L-1。若保持溫度不變,將密閉容器的容積壓縮為原來的1/2,達到新的平衡時C的濃度為1.8x mol·L-1。下列說法正確的是( )
nC(g),1 min時達到平衡,C的濃度為x mol·L-1。若保持溫度不變,將密閉容器的容積壓縮為原來的1/2,達到新的平衡時C的濃度為1.8x mol·L-1。下列說法正確的是( )
A.化學計量數的關系為2+m <n
B.容器的容積縮小,正反應速率增大,逆反應速率減小
C.原容器中用B表示的該反應在1min內的平均速率為![]() mol·(L·min)-1
mol·(L·min)-1
D.若保持溫度和容器容積不變,充入氦氣,平衡向逆反應方向移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有下列化學反應,按要求回答問題:
A.(NH4)2SO3![]() 2NH3↑+H2O+SO2↑ B.2CO+O2
2NH3↑+H2O+SO2↑ B.2CO+O2![]() 2CO2
2CO2
C.2C+SiO2![]() Si+2CO↑ D.NH4NO3
Si+2CO↑ D.NH4NO3![]() N2O+ 2H2O
N2O+ 2H2O
E.CaCO3 + CO2+ H2O=Ca(HCO3)2 F.MnO2 + 4HCl(濃) ![]() MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
(1)以上反應中,屬于氧化還原反應的是________________(填上述反應的編號);
(2)在反應MnO2 + 4HCl(濃) ![]() MnCl2 + Cl2↑+ 2H2O中:
MnCl2 + Cl2↑+ 2H2O中:
①氧化劑是___________,氧化產物是________。
②在該反應方程式中用雙線橋法表示出電子轉移的方向和數目_______________。
③若產生了標準狀況下3.36L的氯氣,則被氧化的HCl的物質的量為________摩爾。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com