
碳、氮和鋁的單質及其化合物在工農業生產和生活中有重要用途。
(1)真空碳熱還原—氧化法可實現由鋁礦制備金屬鋁,其相關的熱化學方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g) △H=akJ·mol-1
3AlCl(g)═2Al(l)+AlCl3(g) △H=bkJ·mol-1
反應Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=_________kJ·mol-1(用含a、b的代數式表示);
(2)用活性炭還原法可以處理氮氧化物。某研究小組向某密閉容器中加入一定量的活性炭和NO,發生反應C(s)+2NO(g) N2(g)+CO2(g) △H=Q kJ·mol-1。在T1℃時,反應進行到不同時間測得各物質的濃度如下:
N2(g)+CO2(g) △H=Q kJ·mol-1。在T1℃時,反應進行到不同時間測得各物質的濃度如下:
時間 物質 | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
①0~10min內,NO的平均反應速率v(NO)=___________,T1℃時,該反應的平衡常數K=_______
②30min后,只改變某一條件,反應重新達到平衡,根據上表中的數據判斷改變的條件可能是__________(填字母編號)。
a.通入一定量的NO b.通入一定量的N2
c.適當升高反應體系的溫度 d.加入合適的催化劑
e.適當縮小容器的體積
③在恒容條件下,能判斷該反應一定達到化學平衡狀態的依據是_________(填選項編號)。
a.單位時間內生成2nmolNO(g)的同時消耗nmolCO2(g)
b.反應體系的壓強不再發生改變
c.混合氣體的密度保持不變
d.混合氣體的平均相對分子質量保持不變
④若保持與上述反應前30min的反應條件不變,起始時NO的濃度為2.50mol/L,則反應達平衡時c(NO)=_______ mol/L。NO的轉化率_______(填“增大”、“減小”或“不變”)。
 每課必練系列答案
每課必練系列答案科目:高中化學 來源:湖南省長沙市2016-2017學年高一上學期期末考試化學試卷 題型:選擇題
下列各圖示中能較長時間看到Fe(OH)2白色沉淀的是

A. ①②③ B. ①②④ C. ①②③④ D. ②③④
查看答案和解析>>
科目:高中化學 來源:2017屆福建省晉江市等四校高三第二次聯合考試理綜化學試卷(解析版) 題型:選擇題
a、b、c、d為原子序數依次增大的短周期元素,c?的電子層結構與氖相同,化合物ac易溶于常見液體a2b,d的化合物灼燒時火焰呈黃色,下列有關敘述錯誤的是( )
A. 元素的非金屬性次序為c>b>a B. d和其他3種元素均能形成離子化合物
C. 化合物acb中c元素的化合價為+1價 D. 元素a、b、d組成的固體化合物中存在離子鍵和共價鍵
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省南昌市高二上學期期末考試化學試卷(解析版) 題型:選擇題
下列過程中所發生的化學變化屬于取代反應的是
A. 乙炔通入溴水中 B. 乙烯通入酸性高錳酸鉀溶液中
C. 在鎳作催化劑的條件下,苯與氫氣反應 D. 乙烷與氯氣光照下發生反應
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省南昌市高二上學期期末考試化學試卷(解析版) 題型:選擇題
公元前一世紀,我國已使用天然氣,天然氣的主要成分為甲烷。下列關于甲烷的敘述中,錯誤的是
A. 通常情況下,甲烷跟強酸、強堿、強氧化劑不起反應
B. 甲烷化學性質比較穩定,不能被任何氧化劑氧化
C. 甲烷跟氧氣反應無論生成CH3Cl、CH2Cl、CHCl3還是CCl4,都屬于取代反應
D. 甲烷的四種取代物都難溶于水
查看答案和解析>>
科目:高中化學 來源:2016-2017學年廣東省揭陽市高二下學期第一次月考理科綜合化學試卷(解析版) 題型:選擇題
下圖是幾種常見有機物之間的轉化關系,有關說法正確的是( )

A. 有機物a只能是淀粉
B. 反應①、②、③均為取代反應
C. 有機物c可以使酸性高錳酸鉀溶液褪色
D. 有機物d的羧酸類同分異構體只有1種
查看答案和解析>>
科目:高中化學 來源:2017屆江西省、臨川一中高三1月聯考理綜化學試卷(解析版) 題型:填空題
鉻是人體必需的微量元素,鉻元素形成的化合物很多,常見的有Cr2O3、(NH4)2Cr2O7、[Cr(CH3COO)2]2•2H2O等,請回答下列問題:
(1)鉻熔點較高,一般應用鋁熱反應制備鉻單質。寫出利用Cr2O3制備單質鉻的化學方程式 ____________________ 。
(2)實驗室常用Fe2+處理含(NH4)2Cr2O7的廢水,其流程如下:
Cr2O72﹣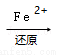 Cr3+
Cr3+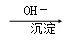 Cr(OH)3↓
Cr(OH)3↓
①(NH4)2Cr2O7中鉻的化合價為 ________ 。
②第一步的離子方程式為_____ 。
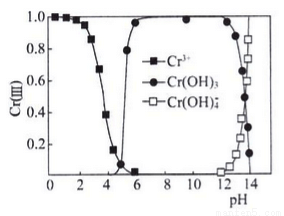
③已知三價鉻[Cr(III)]在水溶液中的存在形態隨pH的變化如下圖,為盡可能除去鉻元素實現廢水達標排放,pH要控制在_______;若pH過高,溶液中殘留鉻量增大,其原因是 __________
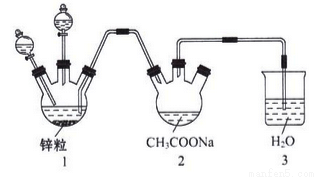
(3)醋酸亞鉻水合物{[Cr(CH3COO)2]2•2H2O,相對分子質量為376} 是常用的氧氣吸收劑。實驗室中以鋅粒、三氯化鉻溶液、醋酸鈉溶液和鹽酸為制備醋酸亞鉻水合物,其裝置如圖所示,且儀器1中預先加入鋅粒。
已知二價鉻不穩定,極易被氧氣氧化,不與鋅反應。制備過程中發生的相關反應如下:
a.Zn+2HCl═ZnCl2+H2↑
b.Zn+2CrCl3═2CrCl2+ZnCl2
c.2Cr2++4CH3COO?+2H2O═[Cr(CH3COO)2]2•2H2O↓
①以上發生的反應中,屬于氧化還原反應的是_______(填序號)。
②往儀器1中加入鹽酸和三氯化鉻溶液的順序是先加入鹽酸一段時間后再加入三氯化鉻溶液,然后再加入鹽酸。這樣做的主要目的是____________________。
③已知其他反應物足量,實驗時取用的CrCl3溶液中含溶質9.51g,取用的醋酸鈉溶液為1.5L0.1mol•L-1實驗后得干燥純凈的[Cr(CH3COO)2]2•2H2O 9.48 g,則該實驗所得產品的產率為 __________(保留兩位有效數字)。
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省、溧水高級中學)等六校高三2月聯考化學試卷(解析版) 題型:選擇題
下列根據實驗操作和現象所得出的結論正確的是
選項 | 實驗操作及現象 | 結論 |
A | 測定等物質的量濃度的Na2CO3和Na2SO3溶液的pH,前者pH比后者的大 | 非金屬性:S>C |
B | 向苯酚濁液中滴加Na2CO3溶液,濁液變澄清 | CO32-結合質子能力比C6H5O-強 |
C | 向10 mL 0.2 mol·L-1NaOH溶液中滴入2滴0.1 mol·L-1MgCl2溶液,產生白色沉淀后,再滴加2滴0.1 mol·L-1FeCl3溶液,白色沉淀轉化為紅褐色沉淀 | 相同溫度下的Ksp:Mg(OH)2>Fe(OH)3 |
D | 將KI和FeCl3溶液在試管中混合后,加入CCl4,振蕩、靜置,下層溶液顯紫紅色 | Fe3+的氧化性大于I2 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com