
【題目】碲是VIA族元素,其單質和化合物在化工生產等方面具有廣泛地應用。
(1)TeO2是兩性氧化物,微溶于水,可溶于強酸或強堿。TeO2和NaOH溶液發生反應的離子方程式為_________________________________。
(2)碲酸(H6TeO6)是一種很弱的酸,Ka1=1×10-7,該溫度下,0.1mol/L H6TeO6的電離度a為_____________(結果保留1位有效數字)。
(3)從粗銅精練的陽極泥(主要含有Cu2Te)中提取粗碲的一種工藝流程如圖:

①已知加壓酸浸時控制溶液的pH為5.0,生成TeO2沉淀。如果H2SO4溶液濃度過大,產生的后果是____________________________。
②“加壓酸浸”中為什么要加壓?_______________________________。
③對濾渣“酸浸”后,將Na2SO3加入Te(SO4)2溶液中進行“還原”得到固態碲,該反應的離子方程式是_________________________________。
④“還原”得到固態碲后分離出粗碲的方法是_______,對粗碲進行洗滌,判斷洗滌干凈的實驗操作和現象是______________________________________。
已知陽極泥中Cu2Te的含量為a%,則m噸陽極泥理論上可制得純度為n%的粗碲___噸。
【答案】 TeO2+2OH=TeO32-+H2O 0.1% TeO2會繼續與酸反應,導致TeO2沉淀不完全 加快溶解速率,有利于反應向生成TeO2的方向進行 2SO32-+ Te4++2H2O=Te↓+2SO42-+4H+ 過濾 取少量最后一次洗滌液,加入BaCl2溶液,若沒有白色沉淀生成,則說明洗滌干凈 ![]()
【解析】(1)TeO2是兩性氧化物,和NaOH溶液反應生成鹽Na2TeO3和水,發生反應的離子方程式為TeO2+2OH=TeO32-+H2O;
(2) H6TeO6![]() H5TeO6-+H+
H5TeO6-+H+
起始濃度(mol/L) 0.1 0 0
變化濃度(mol/L) 0.1α 0.1α 0.1α
平衡濃度(mol/L) 0.1(1-α) 0.1α 0.1α
Ka1=1×10-7=[0.1α×0.1α]/[0.1(1-α)],解得:α=0.1%;
(3)①TeO2具有兩性,如果溶液酸性過強,TeO2會繼續與酸反應,導致TeO2沉淀不完全;②加壓可以加快溶解速率,有利于反應向生成TeO2的方向進行;③Na2SO3加入Te(SO4)2溶液中進行還原得到固態碲,同時生成Na2SO4,該反應的離子方程式是 2SO32-+Te4+ +2H2O=Te↓+2SO42-+4H+;④通過過濾從反應后的混合液中獲得粗碲,粗碲表面附著的離子中含有SO42-,因此判斷洗滌干凈的實驗操作和現象是:取少量最后一次洗滌液,加入BaCl2溶液,若沒有白色沉淀生成,則說明洗滌干凈。已知陽極泥中Cu2Te的含量為a%,則根據原子守恒可知m噸陽極泥理論上可制得純度為n%的粗碲![]() 噸。
噸。


 提分百分百檢測卷系列答案
提分百分百檢測卷系列答案 寶貝計劃期末沖刺奪100分系列答案
寶貝計劃期末沖刺奪100分系列答案科目:高中化學 來源: 題型:
【題目】Ⅰ.CH4和CO2可以制造價值更高的化學產品。已知:
CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) ΔH 1=a kJ/mol
CO2(g)+2H2O(g) ΔH 1=a kJ/mol
CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH 2=b kJ/mol
CO2(g)+H2(g) ΔH 2=b kJ/mol
2CO(g)+O2(g)![]() 2CO2(g) ΔH 3=c kJ/mol
2CO2(g) ΔH 3=c kJ/mol
(1)求反應CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) ΔH = kJ/mol(用含a、b、c的代數式表示)。
2CO(g)+2H2(g) ΔH = kJ/mol(用含a、b、c的代數式表示)。
(2)一定條件下,等物質的量的(1)中反應生成的氣體可合成二甲醚(CH3OCH3),同時還產生了一種可參與大氣循環的無機化合物,該反應的化學方程式為 。
(3)用Cu2Al2O4做催化劑,一定條件下發生反應:CO2(g)+CH4(g)![]() CH3COOH(g),溫度與催化劑的催化效率和乙酸的生成速率的關系如圖,回答下列問題:
CH3COOH(g),溫度與催化劑的催化效率和乙酸的生成速率的關系如圖,回答下列問題:
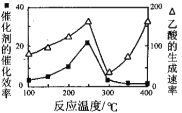
①250~300℃時,乙酸的生成速率降低的原因是 。
②300~400℃時,乙酸的生成速率升高的原因是 。
Ⅱ.鈉硫電池以熔融金屬Na、熔融S和多硫化鈉(Na2Sx )分別作為兩個電極的反應物,多孔固體Al2O3陶瓷(可傳導Na+)為電解質,其反應原理如圖所示:
Na2Sx ![]() 2Na+xS (3<x<5)
2Na+xS (3<x<5)
物質 | Na | S | Al2O3 |
熔點/℃ | 97.8 | 115 | 2050 |
沸點/℃ | 892 | 444.6 | 2980 |

(4)根據上表數據,判斷該電池工作的適宜溫度應為 (填字母序號)。
A.100℃以下
B.100℃~300℃
C.300℃~350℃
D.350℃~2050℃
(5)關于鈉硫電池,下列說法正確的是 (填字母序號)。
A.放電時,電極A為負極
B.放電時,Na+的移動方向為從B到A
C.充電時,電極A應連接電源的正極
D.充電時電極B的電極反應式為![]() 2e
2e![]() xS
xS
(6)25℃時,若用鈉硫電池作為電源電解500mL 0.2mol/L NaCl溶液,當溶液的pH變為13時,電路中通過的電子的物質的量為 mol,兩極的反應物的質量差為 g。(假設電解前兩極的反應物的質量相等)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用NA表示阿伏加德羅常數的數值,下列說法錯誤的是
A. l00mL1mol/LNa2SO4溶液中溶質離子總數為0.3NA
B. 常溫下,22.4LH2O含有10NA個電子
C. 常溫下,46gNO2和N2O4的混合氣體中含有的氮原子數目為NA
D. 若120g石墨能寫a個字,則平均每個字約含有![]() 個碳原子
個碳原子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數,下列敘述正確的是( )
A. 烷烴中除甲烷外,很多都能使酸性KMn04溶液的紫色褪去
B. 15g甲基(﹣CH3)含有的電子數是9NA
C. 7.8g苯中含有的碳碳雙鍵數為0.3NA
D. 標準狀況下,2.24 L CCl4中的原子總數為0.5NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,硫的某種含氧酸H2SOx(x≤4)與H2S可發生如下反應:H2S+H2SOx—S+(x-3)SO2+H2O(未配平)下列推斷合理的是
A. 該反應中,一定有SO2 B. 該反應中,H2S作還原劑,H2SOx作氧化劑
C. 若x=3,則還原劑與氧化劑的物質的量之比為1:1 D. 若x=4,每生成1molS,轉移的電子為6mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】空氣中含有吸入顆粒物PM2.5,嚴重影響人的生理和健康,因此改善發質結構、機動車輛措施能有效減少PM2.5、SO2、NO3等的污染。請回答下列問題:
(1)將一定量的某PM2.5樣品用蒸餾水溶解制成待測試樣(忽略OH-)。常溫下,測得該試樣的組成及其濃度如下表:
離子 | K+ | Na+ | NH4+ | SO42- | NO3﹣ | Cl﹣ |
濃度/mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根據表中數據判斷,該試樣的pH = ________。
(2)汽車尾氣中NOx和CO的生成。已知:氣缸中生成NO的反應為N2(g)+O2(g)![]() 2NO(g) △H>0。恒溫,恒容密閉容器中,下列敘述,能說明該反應達到化學平衡狀態的是________ (填序號)。
2NO(g) △H>0。恒溫,恒容密閉容器中,下列敘述,能說明該反應達到化學平衡狀態的是________ (填序號)。
A.混合氣體的密度不再變化 B.混合氣體的平均分子質量不再變化
C.N2、O2、NO的物質的量之比為1:1:2 D.氧氣的轉化率不再變化
E.生成lmol N2的間時有lmol O2被消耗
(3)為減少CO2、SO2的排放,常采取的措施如下:
①將煤轉化為淸潔氣體燃料。己知:H2(g)+1/2O2(g)= H2O(g) △H =-241.8kJ mol-1; C(s)+1/2O2(g)=CO(g) △H =-110.5kJ mol-1。寫出焦炭與水蒸氣反應的熱化學方程式:_____________________________________。
②洗滌含SO2的煙氣。下列物質,可作為洗滌含SO2煙氣的洗滌劑的是______(填序號)。
A.濃氨水 B.碳酸氫鈉飽和溶液 C.FeCl3飽和溶液 D.酸性CaCl2飽和溶液
(4)某濕度下,反應2NO(g)+O2(g) ![]() 2NO2(g)中,在保證O2濃度不變的情況下,增大容器的體積, 平衡將_____(填“正反應方向” “逆反應方向”或“不”)移動。
2NO2(g)中,在保證O2濃度不變的情況下,增大容器的體積, 平衡將_____(填“正反應方向” “逆反應方向”或“不”)移動。
判斷的依據是__________________________________。
(5)甲醇燃料電池可能成為未來便攜電子產品應用的主流。某種甲醇燃料電池的工作原理如圖14所示,則通入a氣體的電極,電極反應式為_________________。

(6)—定條件下,甲醇與一氧化碳反應可以合成乙酸。常溫條件下,將a mol/L的CH3COOH溶液與bmol/LBa(OH)2溶液等體積混合,反應平衡時,2c(Ba2+)=c(CH3COO-),用含a和b的代數式表示,該混合溶液中醋酸的電離常數為___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A. 含金屬元素的離子都是陽離子
B. 利用丁達爾現象可以區分溶液和膠體
C. 某元素從游離態變為化合態時,該元素可能被氧化
D. 同溫同壓下,相同體積的氣體含有相同數目的分子數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】黃樟腦(結構簡式如下圖)可作為洋茉莉和香蘭素的原料,能除肥皂的油脂臭,常作廉價的香料使用于皂用香精中。下列有關敘述正確的是

A. 黃樟腦屬于酯、烯烴、芳香族化合物
B. 黃樟腦分子中最少有9個碳原子共面
C. 黃樟腦與H2、Br2均能發生加成反應
D. 與黃樟腦互為同分異構體且含苯環、羧基及一個支鏈的結構有3種
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com