
分析 根據核內質子數=核外核外電子數-電荷數,中子數=質量數-質子數,計算X原子中子數,進而計算每個DmX分子含有中子數,根據n=$\frac{m}{M}$計算DmX的物質的量,結合每個分子含有中子數計算.
解答 解:某元素的一種同位素離子Xm-的質量數為A,核內質子數=b-m,則中子數為(A-b+m),則每個DmX分子含有中子數為(A-b+m+m),ag HmX的物質的量為$\frac{ag}{(A+2m)g/mol}$=$\frac{a}{A+2m}$mol,故含有中子物質的量為$\frac{a}{A+2m}$(A-b+2m)mol;
故答案為:$\frac{a}{A+2m}$(A-b+2m).
點評 本題主要考查了質子數、中子數、質量數、核外電子數之間的關系,難度不大,把握陰離子中核外電子數的計算方法是解題的關鍵.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題

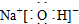 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一定有乙烷 | B. | 一定有丙烷 | ||
| C. | 可能是乙烷和丙烷的混合物 | D. | 可能是甲烷和丁烷的混合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
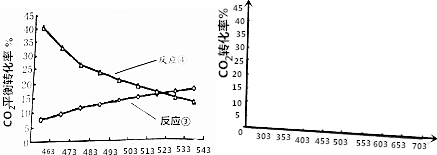
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
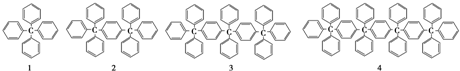
| A. | C158H118 | B. | C158H116 | C. | C160H116 | D. | C160H118 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A | C | |
| B |
| A. | A、B、C三元素的氣態氫化物溶于水均顯酸性 | |
| B. | A、B兩種元素的氣態氫化物均能與它們的最高價氧化物對應的水化物發生反應,且反應類型相同 | |
| C. | C在周期表中的位置為第二周期第ⅦA族,最高價為+7價 | |
| D. | B02是酸性氧化物,AO2不是酸性氧化物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2.4g金屬鎂變為鎂離子時失去的電子數為0.1NA | |
| B. | 1molHCl氣體中的粒子數與0.5 mo1/L鹽酸中溶質粒子數相等 | |
| C. | 6.4g銅與足量的硫磺在絕隔空氣的條件下反應,電子轉移的數目為0.1NA | |
| D. | 1mol白磷分子中所含共價鍵數為4NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com