
分析 A、B、C、D四種原子序數依次增大的短周期元素,A的基態原子2p能級有3個單電子,原子核外電子排布為1s22s22p3,則A為N元素;C的基態原子2p能級級有1個單電子,原子序數大于N元素,故原子核外電子排布為1s22s22p5,則C為F元素,B原子序數介于N、F元素之間,則B為O元素;D的價電子數為2,原子序數大于F元素,處于第三周期ⅡA族,故D為Mg,據此解答.
解答 解:A、B、C、D四種原子序數依次增大的短周期元素,A的基態原子2p能級有3個單電子,原子核外電子排布為1s22s22p3,則A為N元素;C的基態原子2p能級級有1個單電子,原子序數大于N元素,故原子核外電子排布為1s22s22p5,則C為F元素,B原子序數介于N、F元素之間,則B為O元素;D的價電子數為2,原子序數大于F元素,處于第三周期ⅡA族,故D為Mg.
(1)D為Mg,基態原子的電子排布式為1s22s22p63s2,故答案為:1s22s22p63s2;
(2)A的單質為N2,結構式為N≡N,分子中有1個σ鍵、2個π鍵,故答案為:1;2;
(3)同周期隨原子序數增大,元素電負性增大,故電負性F>O>N,B元素的氫化物為H2O,水分子之間存在氫鍵,沸點是同族元素中最高的,故答案為:F>O>N;水分子之間存在氫鍵;
(4)A的最簡單氫化物分子為NH3,分子中N原子成3個σ鍵、含有1對孤對電子,雜化軌道數目為4,N原子采取sp3雜化,故答案為:sp3.
點評 本題是對物質結構的考查,涉及核外電子排布、化學鍵、電負性、氫鍵、雜化方式等,比較基礎,有利于基礎知識的鞏固.


科目:高中化學 來源: 題型:選擇題
| A. | 25℃時,在水中的溶解度NaHCO3大于Na2CO3 | |
| B. | 用Ba(OH)2溶液能鑒別碳酸鈉和碳酸氫鈉溶液 | |
| C. | 受熱時,NaHCO3比Na2CO3容易分解 | |
| D. | NaHCO3和Na2CO3各1mol分別與過量鹽酸充分反應,產生CO2的質量不同 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
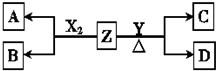 短周期元素組成的單質X2,Y.常溫下,X2是一種黃綠色氣體,Y為淡黃色固體,Z是一種常見的堿,焰色反應呈淺紫色(透過鈷玻璃)且0.1mol•L-1 Z的水溶液pH=13.X2、Y 和Z之間有如圖轉化關系(其他無關物質已略去)
短周期元素組成的單質X2,Y.常溫下,X2是一種黃綠色氣體,Y為淡黃色固體,Z是一種常見的堿,焰色反應呈淺紫色(透過鈷玻璃)且0.1mol•L-1 Z的水溶液pH=13.X2、Y 和Z之間有如圖轉化關系(其他無關物質已略去)查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
 如圖,A池用石墨電極電解NaOH,B池精煉粗銅,一段時間后停止通電,A池中D極產生具有氧化性的氣體在標準狀況下為2.24L.下列說法正確的是( )
如圖,A池用石墨電極電解NaOH,B池精煉粗銅,一段時間后停止通電,A池中D極產生具有氧化性的氣體在標準狀況下為2.24L.下列說法正確的是( )| A. | 圖中電源左側電極為正極 | |
| B. | f應為粗銅板材料 | |
| C. | B池中e質量增加12.8g | |
| D. | 若B池中電解液為CuSO4溶液,則停止通電后,A、B兩池中溶質的物質的量均不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 molH2和16gO2 | B. | NA個N2和11gCO2 | ||
| C. | 18gH2O和1molBr2 | D. | 22.4 LH2(標準狀況)和0.1NACO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 如圖所示裝置,電流表G發生偏轉,同時X極逐漸變粗,Y極逐漸變細,Z是電解質溶液,則X、Y、Z應是下列各組中的( )
如圖所示裝置,電流表G發生偏轉,同時X極逐漸變粗,Y極逐漸變細,Z是電解質溶液,則X、Y、Z應是下列各組中的( )| A. | X是Zn,Y是Cu,Z為稀H2SO4 | B. | X是Cu,Y是Zn,Z為稀H2SO4 | ||
| C. | X是Fe,Y是Ag,Z為稀AgNO3溶液 | D. | X是Ag,Y是Fe,Z為稀AgNO3溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com