
| 物質 | 熔點/℃ | 沸點/℃ | 化學性質 |
| S | 112.8 | 444.6 | 略 |
| S2Cl2 | -77 | 137 | 遇水生成HCl、SO2、S 3000C以上完全分解 |

| 實驗步驟 | 實驗現象和結論 |
| 1.取少量溶液于試管中,滴入幾滴KMnO4溶液 | KMnO4溶液顏色由紫色變綠色,說明溶液中大量存在SO32- |
| 2.另取少量溶液于試管中,加入2-3滴酚酞溶液 | 溶液顏色由無色變紅,說明溶液中大量存在OH- |
| 3.另取少量溶液于試管中,加入足量1mol•L-1HNO3,再加入少量AgNO3溶液 | 仍有白色沉淀產生,說明溶液中大量存 |
分析 (1)S2Cl2遇水生成HCl、SO2、S,在G中生成的 S2Cl2易與H中擴散過來的水蒸氣反應而變質,故應在G和H之間增加干燥裝置;
(2)B中發生反應的離子方程式是濃鹽酸與二氧化錳制取氯氣;E中反應是氯氣和硫發生反應生成二氯化二硫;
(3)根據裝置圖可知儀器B的名稱;實驗中制得的氯氣中含有氯化氫和水蒸汽雜質,與硫反應時必須將其除去,氯氣在飽和食鹽水中溶解度很小,所以用飽和食鹽水可除去氯氣中氯化氫;根據S2Cl2的沸點可知,E裝置中S2Cl2呈氣態,G裝置中S2Cl2呈固態;
(4)S2Cl2遇水生成HCl、SO2、S,可以推知S2Cl2溶于足量的NaOH溶液中,會生成 NaCl、Na2SO3、S,據此答題;
(5)①硫易溶于CS2,用CS2可以把硫從混合物質中萃取出來;
②將兩種互不相溶的液體分離子通常用分液的方法;
③溶液中的陰離子為 OH-和Cl-,根據題中提供的試劑可知,用指示劑檢驗OH-,用硝酸酸化的AgNO3溶液檢驗Cl-.
解答 解:(1)因S2Cl2遇水生成HCl、SO2、S,在G中生成的 S2Cl2易與H中擴散過來的水蒸氣反應而變質,故應在G和H之間增加干燥裝置;
故答案為:在G和H之間增加干燥裝置;
(2)B中發生反應的離子方程式是濃鹽酸與二氧化錳制取氯氣的離子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;E中反應是氯氣和硫發生反應生成二氯化二硫,E中反應的化學方程式由信息可得:2S+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$S2Cl2,
故答案為:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;2S+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$S2Cl2;
(3)根據裝置圖可知儀器B的名稱為圓底燒瓶,實驗中制得的氯氣中含有氯化氫和水蒸汽雜質,與硫反應時必須將其除去,氯氣在飽和食鹽水中溶解度很小,所以用飽和食鹽水可除去氯氣中氯化氫,根據S2Cl2的沸點可知,E裝置中S2Cl2呈氣態,G裝置中S2Cl2呈固態,所以粗S2Cl2產品收集在裝置G中,
故答案為:圓底燒瓶;除去氯氣中的氯化氫氣體;G;
(4)S2Cl2遇水生成HCl、SO2、S,可以推知S2Cl2溶于足量的NaOH溶液中,會生成 NaCl、Na2SO3、S,發生的反應化學方程式為2S2Cl2+6NaOH═4 NaCl+Na2SO3+3H2O+3S↓,
故答案為:2S2Cl2+6NaOH═4 NaCl+Na2SO3+3H2O+3S↓;
(5)①硫易溶于CS2,用CS2可以把硫從混合物質中萃取出來,所以該操作為萃取,
故答案為:萃取;
②將兩種互不相溶的液體分離子通常用分液的方法,
故答案為:分液;
③溶液中的陰離子為 OH-和Cl-,根據題中提供的試劑可知,用指示劑檢驗OH-,用硝酸酸化的AgNO3溶液檢驗Cl-,實驗步驟、實驗現象和結論為
| 實驗步驟 | 實驗現象和結論 |
| 2.另取少量溶液于試管中,加入2-3滴酚酞溶液, | 溶液顏色由無色變紅,說明溶液中大量存在 OH- |
| 3.另取少量溶液于試管中,加入足量1mol•L-1HNO3,再加入少量AgNO3溶液 | 仍有白色沉淀產生,說明溶液中大量存 |
| 實驗步驟 | 實驗現象和結論 |
| 2.另取少量溶液于試管中,加入2-3滴酚酞溶液, | 溶液顏色由無色變紅,說明溶液中大量存在 OH- |
| 3.另取少量溶液于試管中,加入足量1mol•L-1HNO3,再加入少量AgNO3溶液 | 仍有白色沉淀產生,說明溶液中大量存 |
點評 本題主要考查了在實驗室中合成S2C12,根據題目信息分析了原因,培養了學生運用知識的能力與解決問題的能力,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | Ba2+、NO3-、Cl-、Na+ | B. | NO3-、Fe3+、Mg2+、SO42- | ||
| C. | Ca2+、Na+、Cl-、SO42- | D. | K+、Cl-、Al3+、OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋁合金的強度和硬度都比純鋁的大 | |
| B. | 鋁制的容器可以貯存濃硫酸或濃硝酸 | |
| C. | 鋁表面的氧化膜可用鹽酸或氫氧化鈉溶液除去 | |
| D. | 將金屬鈉加入到氯化鋁溶液中可制得鋁 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2gH2所含的原子數目為NA | |
| B. | 標準狀況下,22.4L水中含有水分子數為NA | |
| C. | 常溫下,1L0.1mol•L-1的MgCl2溶液中含有的Cl-數為0.2NA | |
| D. | 常溫常壓下,11.2L CH4中含有的氫原子數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | A原子最外層電子數比B原子最外層電子數少 | |
| B. | A的最高價氧化物對應水化物的堿性強于B的最高價氧化物對應水化物的堿性 | |
| C. | 1molA與足量酸反應生成的H2比1molB與足量酸反應生成的H2多 | |
| D. | 常溫時,A、B均能導電,且導電性良好 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A組 | B組 |
| Ⅰ.H-F鍵的鍵能大于H-O鍵的鍵能 | ①HF的沸點比H2O低 |
| Ⅱ.H-H…F氫鍵的鍵能大于O-H…O氫鍵的鍵能 | ②HF比H2O穩定 |
| Ⅲ.HF分子間能形成的氫鍵個數比H2O分子少 | ③HF的沸點比H2O高 |
| Ⅳ.HF分子與水分子可形成氫鍵 | ④HF極易溶于水 |
| A. | I② | B. | Ⅱ③ | C. | Ⅲ① | D. | Ⅲ④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 和
和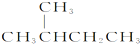
 和
和
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com