
| A. | 0.1mol•L-1 的硫酸溶液中NH4+、Fe2+、Cl-、NO3-可以共存 | |
| B. | 向Ba(OH)2 溶液中滴入硫酸溶液的離子方程式為:Ba2++SO42-═BaSO4↓ | |
| C. | 0.1mol•L-1 AlCl3 溶液,溫度從20℃升高到50℃,所有離子濃度均增大 | |
| D. | pH=11的NaOH 溶液中有:[OH-]=[Na+]+[H+] |
分析 A.硝酸根離子在酸性條件下具有強氧化性,能夠氧化亞鐵離子;
B.氫氧化鋇與稀硫酸反應生成硫酸鋇和水,漏掉了生成水的反應;
C.升高溫度,鋁離子的水解程度增大,鋁離子濃度增大;
D.溶液中一定滿足電荷守恒,根據電荷守恒進行判斷.
解答 解:A.Fe2+、NO3-在酸性條件下發生氧化還原反應,在溶液中不能大量共存,故A錯誤;
B.硫酸與氫氧化鋇反應生成硫酸鋇和水,正確的離子方程式為:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故B錯誤;
C.0.1mol•L-1 AlCl3 溶液,溫度從20℃升高到50℃,鋁離子的水解程度增大,則溶液中鋁離子濃度減小,故C錯誤;
D.pH=11的NaOH溶液中,根據電荷守恒可得:[OH-]=[Na+]+[H+],故D正確;
故選D.
點評 本題考查了離子共存、離子方程式的書寫、離子濃度大小比較等知識,題目難度中等,試題知識點較多、充分考查學生的分析、理解能力及靈活應用基礎知識的能力,注意掌握離子共存、離子方程式的判斷方法,明確判斷離子濃度大小的方法.


 新思維假期作業寒假吉林大學出版社系列答案
新思維假期作業寒假吉林大學出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | 7.8g Na2S和Na2O2的混合物中含有的陰離子數等于0.1NA | |
| B. | 12.5mL 16mol•L-1濃硫酸與足量銅反應,轉移電子數為0.2NA | |
| C. | 5.6 g鐵粉在0.1mol氯氣中充分燃燒,轉移電子數為0.3NA | |
| D. | 1 mol的甲基與1 mol的銨根離子所含電子數均為10NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  | B. | HOOC-COOH | C. | HOCH2CH2OH | D. | CH3COOH |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 金剛烷(C10H16)的結果如圖所示,它可以看成四個等同的六元環組成的空間構型.該金剛烷的二氯代物的數目是( )
金剛烷(C10H16)的結果如圖所示,它可以看成四個等同的六元環組成的空間構型.該金剛烷的二氯代物的數目是( )| A. | 4種 | B. | 5種 | C. | 6種 | D. | 7種 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
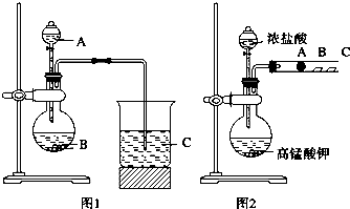
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該溶液中,H+、NH4+、SO42-、Br-可以大量共存 | |
| B. | 該溶液中,Ag+、K+、NO3-、CH3CHO可以大量共存 | |
| C. | 向該溶液中滴入少量FeSO4溶液,反應的離子方程式為:2Fe2++ClO-+2H+═Cl-+2Fe3++H20 | |
| D. | 向該溶液中加入濃鹽酸,每產生1molCl2,轉移電子約為6.02×1023個 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
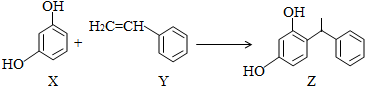
| A. | X、Y和Z均能使溴水褪色 | |
| B. | X和Z均能與NaHCO3溶液反應放出CO2 | |
| C. | Y既能發生取代反應,也能發生加成反應 | |
| D. | Y可作加聚反應單體,X可作縮聚反應單體 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com