
(12分)某學生用0.l000mol.L-l鹽酸標準溶液測定某燒堿樣品的純度(雜質不與鹽酸反應)。實驗步驟如下:
(1)配制待測液:用2.50 g含有少量雜質的固體燒堿樣品配制500 mL溶液。需用的玻璃儀器除了燒杯、膠頭滴管、玻璃棒外,還需要 。
(2)滴定:
I.用蒸餾水洗滌酸式滴定管,并立即注入鹽酸標準溶液至“O”刻度線以上
Ⅱ.固定好滴定管并使滴定管尖嘴充滿液體,調節液面至“0”或“O”刻度線以下,并記錄讀數
Ⅲ.移取20.OOmL待測液注入潔凈的錐形瓶中,并加入2滴酚酞試液
Ⅳ.用標準液滴定至終點,記錄滴定管液面讀數。
①上述滴定步驟中有錯誤的是(填編號) ,該錯誤操作會導致測定結果 (填“偏大”、“偏小”或“無影響”)。
②步驟Ⅳ中滴定時眼睛應 :判斷滴定終點的現象是 。
③若步驟II中仰視讀數,步驟Ⅳ中俯視讀數,則會使測定結果 (填“偏大”、“偏小”或“無影響’')。
(3)按正確操作測得有關數據記錄如下:
| 滴定次數 | 待測液體積 | 標準鹽酸體積(mL) | |
| 滴定前讀數(mL) | 滴定后讀數(mL) | ||
| 第一次 | 20.00 | 0.20 | 20.38 |
| 第二次 | 20.00 | 4.00 | 24.20 |
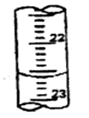
| 第三次 | 20.00 | 2.38 | a |
(12分)(1) 500ml容量瓶(1分) (2)①Ⅰ(2分) 偏大(1分)
②注視錐形瓶中溶液顏色的變化(1分)
溶液由紅色剛好變為無色,且半分鐘內不變色(2分)
③偏小(1分) (3) ①22.60(2分) ②80.8%(2分)
解析試題分析:(1) 配制500ml溶液時,需要500ml容量瓶,所以還需要500ml容量瓶。
(2)①滴定管用水洗滌后,還需要用標準液潤洗,否則相當于稀釋溶液,因此鹽酸的濃度降低,消耗的鹽酸溶液體積偏大,則測定結果偏高。
②步驟Ⅳ中滴定時眼睛應注視錐形瓶中溶液顏色的變化。由于選擇的指示劑是酚酞,所以終點時的現象是溶液由紅色剛好變為無色,且半分鐘內不變色。
③若步驟II中仰視讀數,則讀數偏大。步驟Ⅳ中俯視讀數,讀數偏小,所以消耗溶液的體積偏少,因此測定結果偏小。
(3)根據滴定管的結構可知,此時的讀數應該是a=22.60ml。根據表中數據可知,三次實驗中消耗鹽酸的體積是20.18ml、20.20ml、20.22ml,所以三次實驗的平均值是20.20ml,則氫氧化鈉的物質的量是0.00202mol,則純度是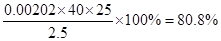 。
。
考點:考查酸堿中和滴定的有關判斷、計算以及有關誤差分析等
點評:判斷中和滴定中的誤差分析的總依據為:由C測==C標V標/V測。由于C標、V待均為定植,所以C測的大小取決于V標的大小,即V標:偏大或偏小,則C測偏大或偏小。根據產生誤差的來源,從以下幾個方面來分析:①洗滌誤差;②讀數誤差;③氣泡誤差;④錐形瓶誤差;⑤變色誤差;⑥樣品中含雜質引起的誤差等,需要具體問題具體分析。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
| 滴定次數 | 鹽酸體積mL | NaOH溶液體積讀數(ml) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 21.30 |
| 2 | 20.00 | 0.00 | 16.30 |
| 3 | 20.00 | 0.00 | 16.22 |
查看答案和解析>>
科目:高中化學 來源: 題型:
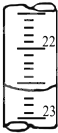 某學生用0.2000mol?L-1的標準NaOH溶液滴定未知濃度的鹽酸,其操作為如下幾步:
某學生用0.2000mol?L-1的標準NaOH溶液滴定未知濃度的鹽酸,其操作為如下幾步:| 滴定次數 | 待測體積(ml) | 標準燒堿體積(ml) | |
| 滴定前讀數 | 滴定后讀數 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 4.00 | 24.00 |
| 第三次 | 20.00 | 2.00 | 24.10 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com