

分析 混有硫酸鈉和碳酸氫鈉的氯化鈉加熱后,碳酸氫鈉受熱分解,得殘留物A中含有硫酸鈉、碳酸鈉、氯化鈉,溶解后得混合溶液B,B中加入氯化鋇溶液生成硫酸鋇沉淀和碳酸鋇沉淀,充分攪拌得懸濁液C,在C中加碳酸鈉除去多余的氯化鋇,過濾得溶液D主要含有氯化鈉另有部分碳酸鈉,經蒸發結晶可得氯化鈉固體,
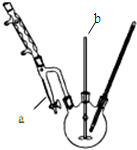
(1)加熱可使碳酸氫鈉分解;灼燒固體應在坩堝中進行;
(2)碳酸鈉、硫酸鈉與氯化鋇生成碳酸鋇、硫酸鋇沉淀,因為碳酸鋇比硫酸鋇易溶,所以碳酸鋇可以轉化成硫酸鋇,據此答題;
(3)判斷SO42-已經除盡,可以在沉淀后的上層清液中檢驗硫酸根離子,可以用氯化鋇;
(4)根據上面的分析可知,目標物質中含有碳酸鈉,可以用鹽酸除去碳酸鈉;
解答 解:混有硫酸鈉和碳酸氫鈉的氯化鈉加熱后,碳酸氫鈉受熱分解,得殘留物A中含有硫酸鈉、碳酸鈉、氯化鈉,溶解后得混合溶液B,B中加入氯化鋇溶液生成硫酸鋇沉淀和碳酸鋇沉淀,充分攪拌得懸濁液C,在C中加碳酸鈉除去多余的氯化鋇,過濾得溶液D主要含有氯化鈉另有部分碳酸鈉,經蒸發結晶可得氯化鈉固體,
(1)加熱可使碳酸氫鈉分解轉化為碳酸鈉,灼燒固體應在坩堝中進行,
故答案為:使碳酸氫鈉分解轉化為碳酸鈉;坩堝;
(2)碳酸鈉、硫酸鈉與氯化鋇生成碳酸鋇、硫酸鋇沉淀,反應的離子方程式為Ba2++CO32-=BaCO3↓、Ba2++SO42-=BaSO4↓,因為碳酸鋇比硫酸鋇易溶,所以碳酸鋇可以轉化成硫酸鋇,所以溶液中離子的濃度大小關系為SO42-<CO32-,
故答案為:Ba2++CO32-=BaCO3↓、Ba2++SO42-=BaSO4↓;<;
(3)判斷溶液B中SO42-已經除盡的方法為用潔凈的試管取少量上層清液,向試管中滴加酸化的氯化鋇溶液,若無沉淀產生,則說明硫酸根離子已經除盡,
故答案為:用潔凈的試管取少量上層清液,向試管中滴加酸化的氯化鋇溶液,若無沉淀產生,則說明硫酸根離子已經除盡;
(4)根據上面的分析可知,目標物質中含有碳酸鈉,改進的方法是在操作④之后加入適量的鹽酸并測定pH值,除去溶液中碳酸根離子,
故答案為:碳酸鈉;在操作④之后加入適量的鹽酸并測定pH值,除去溶液中碳酸根離子.
點評 本題考查了粗鹽的提純、溶液的配制級有關化學方程式的計算等相關知識,側重基礎知識的靈活應用,難度不大.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | 某些館的外殼使用非晶硅薄膜,以充分利用太陽能 | |
| B. | 世博會期間,利用可降解的“主米塑料”替代一次性飯盒,可防止產生白色污染 | |
| C. | 世博會中國館“東方之冠”使用的鋼筋混凝土屬于高分子化合物 | |
| D. | 世博停車場安裝催化光解設施,可將汽車尾氣中的CO和NO 轉化為無毒氣體CO2和N2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2O2能與酸反應生成鹽和水,所以Na2O2是堿性氧化物 | |
| B. | Na2CO3不能轉化成NaHCO3,而NaHCO3能轉化成Na2CO3 | |
| C. | 與相同濃度的酸反應的速率:Na2CO3<NaHCO3 | |
| D. | Na著火時可用泡沫滅火器滅火 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 塑化劑DBP(鄰苯二甲酸二丁酯)主要應用于PVC等合成材料中作軟化劑.反應原理為:
塑化劑DBP(鄰苯二甲酸二丁酯)主要應用于PVC等合成材料中作軟化劑.反應原理為: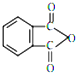 +2CH3CH2CH2CH2OH→
+2CH3CH2CH2CH2OH→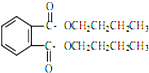 +H2O
+H2O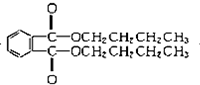 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$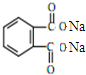 +2CH3CH2CH2CH2OH.
+2CH3CH2CH2CH2OH.查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com