
| 物質 | 氫氣 | 原煤 (主要成份是C) | 汽油 (主要成份C8H18) |
| 熱量(kJ) | 285.8 | 250.9 | 4910 |
分析 Ⅰ.(1)1molH2完全燃燒放出的熱量為:285.8kJ,所以熱化學方程式是2H2(g)+O2(g)=2H2O (l)△H=-571.6 kJ/mol;
(2)H2燃燒放出的熱量大于原煤和汽油,且產(chǎn)物無污染;
(3)電解飽和食鹽水,依據(jù)電極反應判斷生成產(chǎn)物,書寫離子方程式.
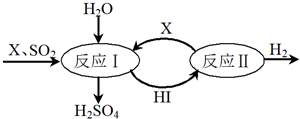
Ⅱ.由圖可知反應Ⅰ是碘單質與二氧化硫反應生成硫酸和氫碘酸,反應Ⅱ是氫碘酸分解生成氫氣和碘單質,由此分析各項;
(1)該過程可循環(huán)利用的物質是I2和HI;
(2)總反應的化學方程式是:SO2+2H2O=H2SO4+H2;
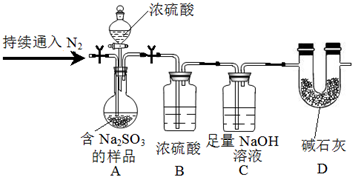
(3)①裝置B是濃硫酸,用來干燥氣體吸收水蒸氣;
②若實驗前后裝置C的質量差為ng,依據(jù)元素守恒計算亞硫酸鈉質量得到質量分數(shù).
解答 解:Ⅰ.(1)1molH2完全燃燒放出的熱量為:285.8kJ,所以熱化學方程式是2H2(g)+O2(g)=2H2O (l)△H=-571.6 kJ/mol,故答案為:2H2(g)+O2(g)=2H2O (l)△H=-571.6 kJ/mol;
(2)H2燃燒放出的熱量大于原煤和汽油,且產(chǎn)物無污染,故答案為:相同條件下,等質量的H2燃燒放出的熱量大于原煤和汽油,產(chǎn)物無污染,可循環(huán)利用;
(3)電解飽和食鹽水,溶液中的氯離子在陽極失電子生成氯氣,氫離子在陰極得到電子生成氫氣,陰極附近氫氧根離子濃度增大生成氫氧化鈉,反應的離子方程式:2Cl-+2H2O$\frac{\underline{\;通電\;}}{\;}$2OH-+H2↑+Cl2↑,故答案為:2Cl-+2H2O$\frac{\underline{\;通電\;}}{\;}$2OH-+H2↑+Cl2↑;
Ⅱ.由圖可知反應Ⅰ是碘單質與二氧化硫反應生成硫酸和氫碘酸,反應Ⅱ是氫碘酸分解生成氫氣和碘單質,
(1)該過程可循環(huán)利用的物質是I2和HI,故答案為:I2和HI;
(2)總反應的化學方程式是:SO2+2H2O=H2SO4+H2,故答案為:SO2+2H2O=H2SO4+H2;
(3)①裝置B是濃硫酸,用來干燥氣體吸收水蒸氣,故答案為:干燥SO2;
②若實驗前后裝置C的質量差為ng,依據(jù)元素守恒計算亞硫酸鈉質量得到質量分數(shù),所需數(shù)據(jù)為:含Na2SO3的樣品質量、裝置C通入SO2 前后的質量,故答案為:含Na2SO3的樣品質量、裝置C通入SO2 前后的質量.
點評 本題考查了熱化學方程式的書寫,電極反應式的書寫和物質成分的實驗設計分析,實驗驗證的方法應用,主要是實驗基本操作,物質性質的分析應用,掌握基礎是關鍵,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 在通常狀況下,新制的氯水呈黃綠色 | |
| B. | 將足量氯水加入到紫色石蕊試液中,溶液只能變成紅色 | |
| C. | 將氯水加入到NaHCO3粉末中,有氣泡產(chǎn)生 | |
| D. | 將氯水加入到硝酸酸化的AgNO3溶液中,有白色沉淀產(chǎn)生 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.5 mol/(L•min) | B. | 2mol/(L•s) | C. | 2mol/(L•min) | D. | 3mol/(L•min) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2NA | B. | NA | C. | 略小于NA | D. | 6.02×1022 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
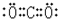 .
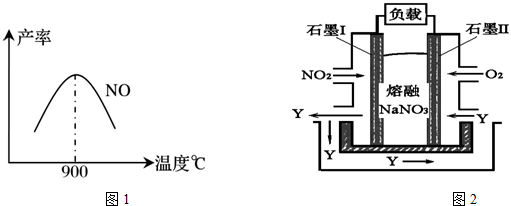
.
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 牛奶經(jīng)工業(yè)發(fā)酵后得到的酸奶 | B. | 用工業(yè)食鹽腌制的泡菜 | ||
| C. | 霉變的大米、花生 | D. | 用甲醛溶液浸泡的海鮮品 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com