
| A. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+NH3•H2O+2BaSO4↓ | |
| B. | 常溫下,0.1 mol•L-1Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| C. | 常溫下,將0.1 mol•L-1CH3COOH溶液加水稀釋,當溶液的pH從3.0升到4.0時,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$的值增大到原來的10倍 | |
| D. | 常溫下,0.1 mol•L-1HA溶液與0.1 mol•L-1NaOH溶液恰好完全反應時,溶液中一定存在:c(Na+)=c(A-)>c(OH-)=c(H+) |
分析 A.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀,說明SO42-與Ba2+的比例是1:2,銨根離子結合氫氧根離子能力大于氫氧化鋁,所以氫氧化鋁不會溶解;
B.根據硫化鈉溶液中的質子守恒判斷;
C.根據醋酸的電離平衡常數可知:$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=$\frac{{K}_{a}}{c({H}^{+})}$,據此判斷稀釋后該比值的變化;
D.HA若為弱酸,則反應后生成強堿弱酸鹽,溶液顯示堿性,則c(Na+)>c(A-)、c(OH-)>c(H+).
解答 解:A.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀,反應生成氫氧化鋁沉淀、一水合氨和硫酸鋇,正確的離子方程式為:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓,故A錯誤;
B.常溫下,0.1 mol•L-1Na2S溶液中,根據質子守恒可得:c(OH-)=c(H+)+c(HS-)+2c(H2S),故B錯誤;
C.常溫下,將0.1 mol•L-1CH3COOH溶液加水稀釋,當溶液的pH從3.0升到4.0時,稀釋過程中醋酸的電離平衡常數不變,氫離子濃度減小為原來的$\frac{1}{10}$,結合醋酸的電離平衡常數可知,$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=$\frac{{K}_{a}}{c({H}^{+})}$,故該比值變為原來的10倍,故C正確;
D.當HA為弱酸時,反應生成強堿弱酸鹽NaA,溶液呈堿性,則:c(Na+)>c(A-)、c(OH-)>c(H+),則溶液中離子濃度大小為:c(Na+)>c(A-)>c(OH-)>c(H+),故D錯誤;
故選C.
點評 本題考查了離子濃度大小比較、離子方程式的書寫、弱電解質的電離及其影響等知識,題目難度中等,試題知識點較多,充分考查了學生的分析、理解能力,注意掌握電荷守恒、物料守恒、質子守恒及鹽的水解原理在判斷離子濃度大小中的應用.


科目:高中化學 來源: 題型:選擇題
| A. | A>B>C>D | B. | A>C>D>B | C. | C>A>B>D | D. | B>D>C>A |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
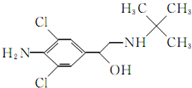 食品安全是現今百姓生活中熱議問題之一,瘦肉精學名鹽酸克倫特羅,白色或類白色的結晶粉末,無臭、味苦,熔點161℃,溶于水、乙醇,微溶于丙酮,不溶于乙醚.其結構簡式如圖.有關瘦肉精的說法不正確的是( )
食品安全是現今百姓生活中熱議問題之一,瘦肉精學名鹽酸克倫特羅,白色或類白色的結晶粉末,無臭、味苦,熔點161℃,溶于水、乙醇,微溶于丙酮,不溶于乙醚.其結構簡式如圖.有關瘦肉精的說法不正確的是( )| A. | 化學式為C12H18ONCl2 | |
| B. | 遇FeCl3溶液發生顯色反應 | |
| C. | 屬于芳香族化合物 | |
| D. | 可以發生取代、加成、水解、酯化、消去反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
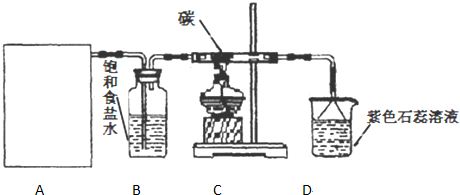
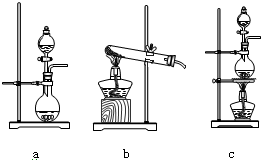
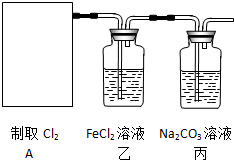
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
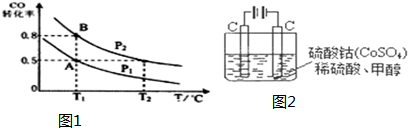
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
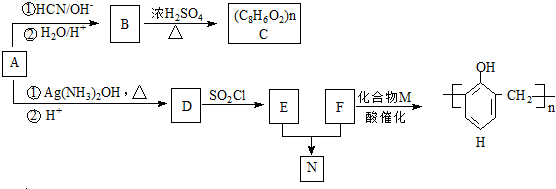
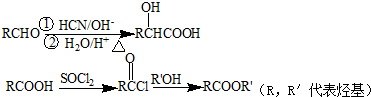 (R,R′代表烴基)
(R,R′代表烴基)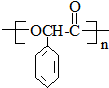 ,M的結構式
,M的結構式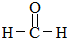 .
. .
.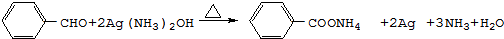 .
.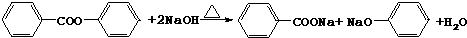 .
.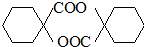 ,其它無機試劑任選.
,其它無機試劑任選.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子序數為34 | B. | 還原性:H2Se<H2S | ||
| C. | 酸性:H2SeO4<HBrO4 | D. | 穩定性:H2Se>AsH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 為了加快反應速率可用飽和食鹽水代替水反應 | |
| B. | 此反應是放熱反應 | |
| C. | 反應中不需加碎瓷片作沸石 | |
| D. | 為了除去雜質氣體,除了用硫酸銅外還可用氫氧化鈉溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com