
| A. | 標準狀況下,22.4LHF中含有的分子數目為NA | |
| B. | .1 L 0.1mol/L 的FeCl3溶液中,Fe3+的數目為0.1NA | |
| C. | .標準狀況下,2.24LCl2溶于水,轉移的電子數目為0.1NA | |
| D. | .5.6gFe在0.1molCl2中充分燃燒,轉移的電子數目為0.2NA |
分析 A、標況下HF為液態;
B、鐵離子是弱堿陽離子;
C、氯氣和水的反應為可逆反應;
D、求出鐵的物質的量,然后根據1molFe~$\frac{3}{2}$molCl2來分析.
解答 解:A、標況下HF為液態,故不能根據氣體摩爾體積來計算其物質的量,故A錯誤;
B、鐵離子是弱堿陽離子,在溶液中會水解,故溶液中的鐵離子的個數小于0.1NA個,故B錯誤;
C、氯氣和水的反應為可逆反應,不能完全反應,故轉移的電子數小于0.1NA個,故C錯誤;
D、5.6g鐵的物質的量為0.1mol,而1molFe~$\frac{3}{2}$molCl2,故0.1mol氯氣要想反應完全,需要0.15mol氯氣,故鐵過量,氯氣能完全反應,由于氯氣反應后變為-1價,故0.1mol氯氣轉移0.2mol電子即0.2NA個,故D正確.
故選D.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 聞名世界的中國陶瓷、釀酒等技術都充分應用了化學工藝 | |
| B. | 四大發明之一黑火藥是由硫黃、硝石、木炭三種物質按一定比例混合制成 | |
| C. | 侯氏制堿法的工藝過程中應用了物質溶解度的差異 | |
| D. | 打磨磁石制作指南針為化學變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

| 沉淀物 | 開始沉淀 | 完全沉淀 |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用SiO2制備硅酸不可能一步完成 | |
| B. | 使用澄清的石灰水可以鑒別Na2CO3和NaHCO3兩種白色固體 | |
| C. | 把鐵粉和銅粉放入FeCl3溶液充分反應后有固體剩余,固體中可能有銅無鐵 | |
| D. | 燒堿溶液應保存在塞有橡膠塞的細口玻璃瓶中 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
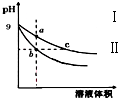 常溫下,相同pH的氫氧化鈉和醋酸鈉溶液加水稀釋,平衡時pH隨溶液體積變化的曲線如圖所示,則下列敘述正確的是( )
常溫下,相同pH的氫氧化鈉和醋酸鈉溶液加水稀釋,平衡時pH隨溶液體積變化的曲線如圖所示,則下列敘述正確的是( )| A. | b、c兩點溶液的導電能力相同 | |
| B. | a、b、c三點溶液中水的電離程度a>c>b | |
| C. | c點溶液中c (H+)=c (OH-)+c (CH3COOH) | |
| D. | 用等濃度的鹽酸分別與等體積的b、c處溶液恰好完全反應,消耗鹽酸體積 Vb=Vc |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 人類歷史上使用最早的合金是青銅 | |
| B. | 目前世界上用量最大的合金是鋼 | |
| C. | 改變原料的配比、改變生成合金的條件,可以得到具有不同性質的合金 | |
| D. | 一般合金的熔點高于它的各成分金屬 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應每脫去1mol Cl2會生成1molSO42- | |
| B. | 脫氯反應后的溶液顯酸性 | |
| C. | 根據該反應可判斷還原性:S2O32->Cl- | |
| D. | 反應中硫元素發生了氧化反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com