
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化學式 | BaSO4 | BaSO3 |
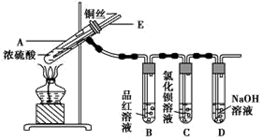
分析 (1)加熱條件下,Cu和濃硫酸發生氧化還原反應生成CuSO4、SO2、H2O,根據反應物、生成物和反應條件書寫方程式;
(2)SO2能和有色物質反應生成無色物質而具有漂白性,SO2能漂白品紅溶液;
(3)SO2具有還原性,能被強氧化劑氧化生成硫酸;SO2屬于酸性氧化物,能和堿溶液反應生成亞硫酸鹽,亞硫酸鹽和BaCl2溶液發生復分解反應.
解答 解:(1)加熱條件下,Cu和濃硫酸發生氧化還原反應生成CuSO4、SO2、H2O,根據反應物、生成物和反應條件知,該反應方程式為Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,故答案為:Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)SO2能和有色物質反應生成無色物質而具有漂白性,SO2能漂白品紅溶液,只要B中溶液褪色就說明銅和濃硫酸發生反應,故答案為:B中品紅溶液褪色;
(3)SO2具有還原性,能被強氧化劑氧化生成硫酸,Cl2具有強氧化性,在水溶液里能將SO2氧化為硫酸,硫酸和BaCl2溶液發生復分解反應生成BaSO4,離子方程式為Cl2+SO2+2H2O=4H++2Cl-+SO42-、Ba2++SO42-=BaSO4↓;SO2屬于酸性氧化物,能和堿溶液反應生成亞硫酸鹽,亞硫酸鹽和BaCl2溶液發生復分解反應生成BaSO3,反應方程式為SO2+2NH3+H2O=(NH4)2SO3、SO32-+Ba2+=BaSO3↓,二氧化硫體現還原性的離子反應方程式為Cl2+SO2+2H2O=4H++2Cl-+SO42-(或Ba2++SO2+Cl2+2H2O=BaSO4↓+4H++2Cl-).
故答案為:BaSO4;BaSO3;Cl2+SO2+2H2O=4H++2Cl-+SO42-(或Ba2++SO2+Cl2+2H2O=BaSO4↓+4H++2Cl-).
點評 本題考查了濃硫酸性質及其應用,題目難度中等,注意掌握二氧化硫、二氧化碳的性質及檢驗方法,明確檢驗順序為解答關鍵,試題培養了學生的分析能力及化學實驗能力.


 一線名師提優試卷系列答案
一線名師提優試卷系列答案 陽光試卷單元測試卷系列答案
陽光試卷單元測試卷系列答案科目:高中化學 來源: 題型:選擇題
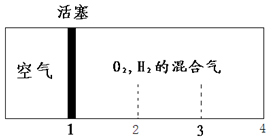 如圖所示裝置,密閉容器內分別充入空氣和H2、O2的混合氣體在可移動的活塞兩邊,在標準狀況下若將H2、O2的混合氣體點燃引爆,活塞先左彈,恢復原溫度后,活塞右滑停留于容器的中央,則原來H2、O2的體積比可能為( )
如圖所示裝置,密閉容器內分別充入空氣和H2、O2的混合氣體在可移動的活塞兩邊,在標準狀況下若將H2、O2的混合氣體點燃引爆,活塞先左彈,恢復原溫度后,活塞右滑停留于容器的中央,則原來H2、O2的體積比可能為( )| A. | 7:2 | B. | 5:4 | C. | 3:1 | D. | 2:7 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
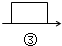 $→_{④}^{Na_{2}CO_{3}}$$→_{⑤}^{()}$濾液$→_{⑥}^{適量鹽酸}$$→_{⑦}^{蒸發、結晶、烘干}$精鹽
$→_{④}^{Na_{2}CO_{3}}$$→_{⑤}^{()}$濾液$→_{⑥}^{適量鹽酸}$$→_{⑦}^{蒸發、結晶、烘干}$精鹽 中填寫所使用除雜試劑的化學式NaOH,在⑤中的操作名稱是過濾.
中填寫所使用除雜試劑的化學式NaOH,在⑤中的操作名稱是過濾.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
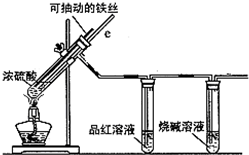 某校化學小組為探究鐵與濃硫酸反應是否生成SO2,設計了以下裝置進行實驗.
某校化學小組為探究鐵與濃硫酸反應是否生成SO2,設計了以下裝置進行實驗.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
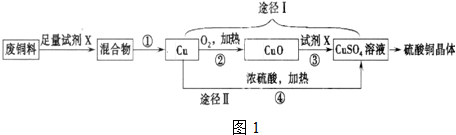

查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
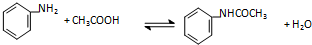
| 物質 | 相對分子質量 | 熔點(℃) | 沸點 | 溶解度(g) | |
| 水 | 乙醇 | ||||
| 苯胺 | 93 | -6 | 184 | 3.42(20℃) | 任意比混溶 |
| 乙酸 | 60 | 17 | 117.9 | 任意比混溶 | 任意比混溶 |
| 乙酰苯胺 | 135 | 114 | 304 | 0.56(20℃) 3.45(50℃) 5.20(100℃) | 36.9(20℃) |

查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
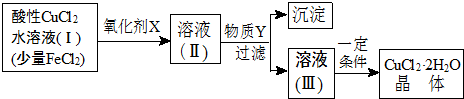
| Fe3+ | Fe2+ | Cu2+ | |
| 氫氧化物開始沉淀時的pH | 1.9 | 7 | 4.7 |
| 氫氧化物完全沉淀時的pH | 3.2 | 9 | 6.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 如圖:A處通入氯氣,關閉B閥時,C處干燥紅色布條無變化,打開B閥時,C處干燥的紅色布條褪色.則下列說法正確的是( )
如圖:A處通入氯氣,關閉B閥時,C處干燥紅色布條無變化,打開B閥時,C處干燥的紅色布條褪色.則下列說法正確的是( )| A. | D中可以盛放濃硫酸 | B. | D中可以盛放飽和食鹽水 | ||
| C. | D中可以盛放水 | D. | A處通入的是干燥的氯氣 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com