
| A. | 反應物的總能量低于生成物的總能量時,一定不能自發進行反應 | |
| B. | 已知:CH4(g)+$\frac{3}{2}$O2(g)═2H2O(l)+CO(g)△H,則△H表示CH4的燃燒熱 | |
| C. | 恒溫恒壓時,將2 mol A和1 mol B投入密閉容器中,發生反應:2A(g)+B(g)?2C(g),充分反應后測得放出的熱量為Q kJ,則該反應的△H=-Q kJ/mol | |
| D. | 由4P(s,紅磷)═P4(s,白磷)△H=+139.2 kJ/mol,可知紅磷比白磷穩定 |
分析 A.吸熱反應可能自發進行;
B、燃燒熱是指完全燃燒1mol物質生成最穩定產物所放出的熱量;
C、可逆反應反應物不能完全轉化;
D、根據反應確定物質的能量高低,物質具有的能量越低越穩定.
解答 解:A、反應物的總能量低于生成物的總能量的反應是吸熱反應,有些吸熱反應能自發進行,故A錯誤;
B、CH4燃燒未生成穩定的氧化物CO2,不屬于燃燒熱,故B錯誤;
C、反應物不能完全轉化,充分反應后測得放出的熱量為Q kJ,則該反應的△H<-Q kJ/mol,故C錯誤;
D、由紅磷轉化為白磷為吸熱反應,所以等質量時,白磷的能量較高,可知紅磷比白磷穩定,故D正確.
故選D.
點評 本題考查化學反應中物質能量與反應熱關系、反應熱計算、化學反應進行方向等,難度不大,注意反應對自發性的理解.


 海淀黃岡名師導航系列答案
海淀黃岡名師導航系列答案 普通高中同步練習冊系列答案
普通高中同步練習冊系列答案科目:高中化學 來源: 題型:解答題
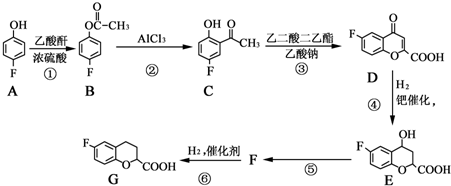
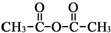
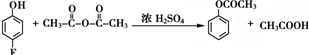 .
.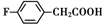 、
、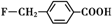
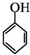 和乙酸酐為原料制備
和乙酸酐為原料制備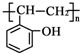 的合成路線流程圖(無機試劑任選).合成路線流程圖示例如下:CH3COOH$→_{△}^{NaOH溶液}$CH3CH2OH$→_{濃硫酸,△}^{CH_{3}COOCH}$CH3COOCH2CH3.
的合成路線流程圖(無機試劑任選).合成路線流程圖示例如下:CH3COOH$→_{△}^{NaOH溶液}$CH3CH2OH$→_{濃硫酸,△}^{CH_{3}COOCH}$CH3COOCH2CH3.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 銅片插A硝酸銀溶液中:Cu+Ag+═Cu2++Ag | |
| B. | 鹽酸滴入澄清石灰水:Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 將金屬Na加入冷水中:2Na+2H2O═2Na+++2OH-+H2↑ | |
| D. | 向含0.5molFeBr2的溶液中通入0.5molC12:2Fe2++C12═2Fe3++2C1- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
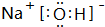 .
.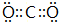 .屬非極性分子(填分子極性).EC2其固體屬原子晶體.
.屬非極性分子(填分子極性).EC2其固體屬原子晶體.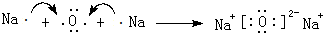 .
.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
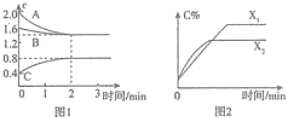
| A. | 0~2分鐘、2~3分鐘內用A濃度表示的平均反應速率:v(0~2)>v(2~3)>0 | |
| B. | 容器中發生的反應可表示為:3A(g)+B(g)?2C(g) | |
| C. | 若X表示溫度,則生成C的反應是放熱反應 | |
| D. | 若其他條件不變,僅減小起始時B的濃度,開始反應后C物質的濃度一定減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在海輪外殼上鑲入鋅塊,可減緩船體的腐蝕速率 | |
| B. | 鐵在潮濕的空氣中容易腐蝕 | |
| C. | 鍍鋅的鐵制品比鍍錫的鐵制品耐用 | |
| D. | 常溫下鋁跟稀硫酸快速反應,跟濃硫酸不反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com