
分析 物質導電的原因:含有自由移動的離子或自由電子;
電解質是指在水溶液里或熔融狀態下能導電的化合物,包括酸、堿、鹽、活潑金屬氧化物和水;
非電解質是在水溶液里和熔融狀態下都不能導電的化合物,包括一些非金屬氧化物、氨氣、大多數有機物(如蔗糖、酒精等);
硫酸氫鈉為強電解質,在水溶液中完全電離出鈉離子、氫離子和硫酸根離子.
解答 解:①Fe含有自由電子,能夠導電;是單質既不是電解質也不是非電解質;
②熔融氫氧化鈉含有自由移動的離子,能夠導電;熔融狀態下能導電的化合物是電解質;
③CO2不含有自由移動的離子或自由電子,不導電;本身不能電離,屬于非電解質;
④乙醇不含有自由移動的離子或自由電子,不導電;在水溶液里和熔融狀態下都不能導電的化合物,是非電解質;
⑤BaSO4不含有自由移動的離子或自由電子,不導電;熔融狀態下能導電的化合物,是電解質;
⑥鹽酸含有自由移動的離子,能夠導電;是混合物既不是電解質也不是非電解質;
⑦NaHSO4固體不含有自由移動的離子或自由電子,不導電;在水溶液里或熔融狀態下能導電的化合物,是電解質;
所以:(1)屬于電解質的是②⑤⑦;
(2)屬于非電解質的是③④;
(3)能導電的是①②⑥;
故答案為:(1)②⑤⑦;
(2)③④;
(3)①②⑥;
(4)硫酸氫鈉為強電解質,在水溶液中完全電離出鈉離子、氫離子和硫酸根離子,電離方程式:NaHSO4=Na++H++SO42-;
故答案為:NaHSO4=Na++H++SO42-.
點評 本題考查了電解質溶液導電的原因及電解質、非電解質判斷,明確電解質、非電解質概念是解題關鍵,注意單質與混合物既不是電解質也不是非電解質,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | ①③⑤ | B. | ④⑤⑥ | C. | ①②④ | D. | ①⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2CO2(g)═2CO(g)+O2(g)△H=+566.0 kJ•mol-1,則 CO(g)的燃燒熱是-283.0kJ•mol-1 | |
| B. | H2SO4和NaOH反應的中和熱△H=-57.3 kJ•mol-1,則1molH2SO4和1molBa(OH)2反應的反應熱△H=-114.6kJ•mol-1 | |
| C. | 石墨轉化為金剛石是吸熱反應,可知金剛石的燃燒熱更大 | |
| D. | 在恒溫時,壓縮容器的體積,則2SO2+O2?2SO3平衡正向移動,該反應的△H減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | KClO3 | B. | KMnO4 | C. | MnO2 | D. | Ca(ClO)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1L 0.1mol/L醋酸 | B. | 0.5L 0.1mol/L H2SO4溶液 | ||
| C. | 1L 0.1mol/L鹽酸 | D. | 2L 0.1mol/L H2SO3溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將100mL 0.1mol•L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3膠粒數目為0.0l NA | |
| B. | Na2O2與足量的水反應生成1 molO2,轉移電子數目為2 NA | |
| C. | 某密閉容器中有2mo1SO2和1mol O2,在一定條件下充分反應,轉移的電子數為4 NA | |
| D. | 18g重水(D2O)所含的電子數為1 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 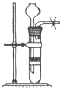 用大理石和鹽酸制取CO2 | B. | 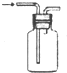 用排氣法收集氨氣 | ||
| C. | 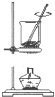 將干海帶灼燒成灰 | D. | 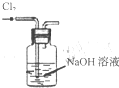 除去Cl2中的HCl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電子總數 | B. | 原子總數 | C. | 質量 | D. | 質子總數 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com