
| A. | NaCl | B. | NaOH | C. | H2 | D. | HCl |
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
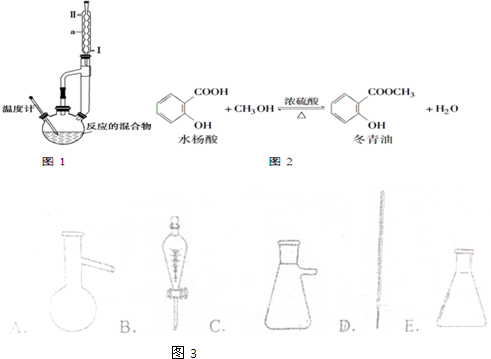
| 相對分 子質量 | 密度/g•cm-3 | 沸點/℃ | 溶解性 | |
| 冬青油 | 152 | 1.180 | 222.2 | 微溶于水 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3:1 | B. | 3:2 | C. | 2:1 | D. | 1:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 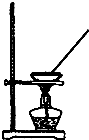 如圖所示裝置獲得碳酸氫鈉固體 | B. | 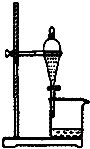 如圖所示裝置分離乙酸和乙酸乙酯 | ||
| C. | 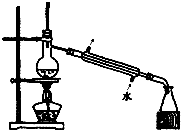 如圖所示裝置制取少量蒸餾水 | D. | 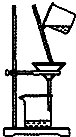 如圖所示裝置提純氫氧化鐵膠體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 增加SO2的濃度 | B. | 充入一定量惰性氣體 | ||
| C. | 升高溫度 | D. | 使用催化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 改變外界條件使化學平衡狀態改變時,平衡常數也一定改變 | |
| B. | 改變條件,反應物的轉化率增大,平衡常數一定增大 | |
| C. | 若一個可逆反應的平衡常數很大,則反應會在較短的時間內完成 | |
| D. | 已知2NO2?N2O4正反應的平衡常數為K1,逆反應的平衡常數為K2,則K1=$\frac{1}{{K}_{2}}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com