
| A. | 水玻璃中通入足量的CO2:SiO32-+2CO2+2H2O═H2SiO3 (膠體)+2CO32- | |
| B. | 氯化亞鐵溶液中通入足量的Cl2:2Fe2++Cl2═2Fe3++2Cl- | |
| C. | NaHCO3溶液中加入足量NaHSO4溶液:2H++CO32-═CO2↑+H2O | |
| D. | 碳酸氫鈉溶液與少量石灰水反應:HCO3-+Ca2++OH-═CaCO3↓+H2O |
分析 A.水玻璃為硅酸鈉溶液,二氧化碳足量,反應生成硅酸沉淀和碳酸氫根離子;
B.氯化亞鐵與氯氣反應生成氯化鐵;
C.碳酸氫根離子不能拆開,應該保留整體形式;
D.石灰水少量,反應生成碳酸鈣沉淀、碳酸鈉和水,碳酸根離子有剩余.
解答 解:A.水玻璃中通入足量的CO2,反應生成硅酸沉淀和碳酸氫鈉,正確的離子方程式為:SiO32-+CO2+H2O═H2SiO3↓+HCO3-,故A錯誤;
B.氯化亞鐵溶液中通入足量的Cl2,反應生成氯化鐵,反應的離子方程式為:2Fe2++Cl2═2Fe3++2Cl-,故B正確;
C.NaHCO3溶液中加入足量NaHSO4溶液,反應生成硫酸鈉、二氧化碳氣體和水,正確的離子方程式為:H++HCO3-═CO2↑+H2O,故C錯誤;
D.碳酸氫鈉溶液與少量石灰水反應生成碳酸鈣沉淀、碳酸鈉和水,正確的離子方程式為:2HCO3-+Ca2++2OH-═CO32-+CaCO3↓+2H2O,故D錯誤;
故選B.
點評 本題考查了離子方程式的書寫判斷,題目難度中等,注意掌握離子方程式的書寫原則,側重考查反應物過量情況對生成物影響,試題培養了學生的分析、理解能力及規范答題能力.


 優生樂園系列答案
優生樂園系列答案科目:高中化學 來源: 題型:選擇題
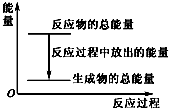
| A. | 反應過程中的能量關系可用如圖表示 | |
| B. | 1 mol Zn的能量大于1 mol H2的能量 | |
| C. | 若將其設計為原電池,則鋅作正極 | |
| D. | 若將其設計為原電池,當有32.5 g Zn溶解時,正極放出的氣體一定為11.2 L |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用水將苯、乙酸、四氯化碳區分開來 | |
| B. | 在實驗室中通常將鈉保存在汽油里 | |
| C. | 用稀硝酸洗去殘留在試管壁上的銀 | |
| D. | 如果苯酚溶液沾到皮膚上,應立即用酒精洗滌 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
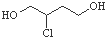 是一種中間產物,下列說法正確的是( )
是一種中間產物,下列說法正確的是( )| A. | 1,3-丁二烯與氫氣加成產物只有一種 | |
| B. | 1,3-丁二烯轉化為 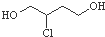 時,先與HCl發生1,2加成再水解得到 時,先與HCl發生1,2加成再水解得到 | |
| C. | 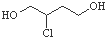 在NaOH醇溶液中或濃硫酸存在時加熱都能發生消去反應 在NaOH醇溶液中或濃硫酸存在時加熱都能發生消去反應 | |
| D. | 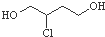 催化氧化得X,X能發生銀鏡反應,則X的結構只有兩種 催化氧化得X,X能發生銀鏡反應,則X的結構只有兩種 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
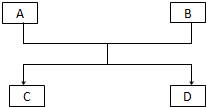 已知A、B、C、D的組成元素都屬于短周期元素,其中A、D為單質,B、C為化合物,它們之間的關系轉化如圖所示,請按要求寫出有關反應式,是離子反應的只寫離子方程式.
已知A、B、C、D的組成元素都屬于短周期元素,其中A、D為單質,B、C為化合物,它們之間的關系轉化如圖所示,請按要求寫出有關反應式,是離子反應的只寫離子方程式.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 充放電時,溶液中Pb2+濃度保持不變 | |
| B. | 放電時轉移2mol電子,消耗2molPb | |
| C. | 放電時的負極反應式為:Pb-2e-═Pb2+ | |
| D. | 充電時的陽極反應式為:Pb2++4OH+2e-═PbO2+2HO |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com