
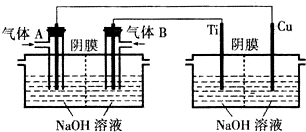
分析 本題探究熱還原法、電解法及干法還原法制備Cu20的原理,其中熱還原法是加熱條件下,利用液態肼(N2H4)還原新制的Cu(OH)2制備Cu20,同時先是氮氣;電解法是利用氫氧燃料電池用銅作陽極電解氫氧化鈉溶液制得Cu20,同時還考查了有關電化學理論,如電極反應式、陰離子的轉移及電極的判斷等;干法還原法是利用反應Cu+CuO$\frac{\underline{\;高溫\;}}{\;}$Cu2O也可制備Cu20,重點考查的是氧化還原反應的分析及運用物質的量進行的計算;
(1)在加熱條件下,用液態肼(N2H4)還原新制的Cu(OH)2制備Cu20,同時放出N2,結合質量守恒定律和氧化還原反應可寫出此反應的化學方程式;
(2)①電解池中銅為陽極,A為原電池的正極,氣體A為氧氣,堿性氫氧燃料電池中,正極上氧氣得電子發生還原反應;
②原電池中,陰離子向負極移動;電解池的陽極是銅電極被氧化,可根據陽極周圍的堿性環境及電解產物來書寫電極反應式;
③電解池中發生的總反應式為2Cu+H2O$\frac{\underline{\;電解\;}}{\;}$Cu20+H2↑,根據電解什么補什么的原則,可知需要補充的物質;
④燃料電池消耗的是氧氣和氫氣,電解池內溶解銅,同時得到氫氣,可知可循環利用的物質為氫氣;
(3)惰性電極電解氯化銅,陽極電極反應為2Cl--2e-=Cl2↑和4OH--4e-=O2↑+2H2O;,陰極電極反應為:Cu2++2e-=Cu和2H++2e-=H2,依據電子守恒和電極反應結合CuCl2溶液中溶質的物質的量計算陽極可得到產物的質量.
解答 解:(1)根據反應物N2H4和Cu(OH)2,生成物是Cu20、H2O和N2,可得化學方程式為4Cu(OH)2+N2H4$\frac{\underline{\;加熱\;}}{\;}$N2↑+2Cu2O+6H2O,
故答案為:4Cu(OH)2+N2H4$\frac{\underline{\;加熱\;}}{\;}$N2↑+2Cu2O+6H2O;
(2)①燃料電池通氧氣的極為正極,連接電解池陽極(銅電極)的極為正確,可知氣體A為氧氣,堿性氫氧燃料電池中,正極上氧氣得電子和水反應生成氫氧根離子,電極反應式為O2+2H2O+4e-=4OH-,
故答案為:O2+2H2O+4e-=4OH-;
②原電池內陰離子向負極移動,故燃料電池內OH-的移動方向為從左向右,電解池陽極是銅被氧化,電極反應式為2Cu+2OH--2e-=Cu2O+H2O,
故答案為:由左向右;2Cu+2OH--2e-=Cu2O+H2O;
③電解池內發生的總反應式為2Cu+H2O$\frac{\underline{\;電解\;}}{\;}$Cu20+H2↑,可知需要補充的物質是水,
故答案為:H2O;
④電解池陰極得到的氫氣可補充燃料電池消耗的氫氣,可見可循環的物質為氫氣,
故答案為:H2;
(3)利用氫氧燃料電池,電解50mL 2mol/L的CuCl2溶液(兩電極為惰性電極),當消耗標況下6.72L氫氣時,n(H2)=$\frac{6.72L}{22.4L/mol}$=0.3mol,n(CuCl2)=0.05L×2mol/L=0.1mol,故陽極產物為Cl2和O2.根據電子守恒可得:n(Cl2)=0.05L×2mol/L=0.1mol和n(O2)=$\frac{0.3mol×2-0.1mol×2}{4}$=0.1mol,故電解池的陽極可得到產物的質量為:0.1mol×71g/mol+0.1mol×32g/mol=10.3g,故答案為:10.3.
點評 本題考查氧化還原反應原理、電化學理論、混合物的計算、守恒計算等,題目難度中等,明確反應過程是解題的關鍵,計算題采取拆分法解答,簡化計算過程,注意在學習中歸納總結.


 新課標階梯閱讀訓練系列答案
新課標階梯閱讀訓練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 將銅插入硝酸銀溶液中:Cu+Ag+═Cu2++Ag | |
| B. | Ca( HCO3)2 溶液與過量 NaOH 溶液反應:HCO3-+OH-+Ca2+═CaCO3↓+H2O | |
| C. | 用食醋除水垢:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| D. | 稀硫酸和Ba(OH)2溶液反應:H++SO42-+Ba 2++OH-═BaSO 4↓+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反應在前50 s的平均速率為v(PCl3)=0.0016mol•L-1•s-1 | |
| B. | 保持其他條件不變,升高溫度,平衡時,c(PCl3)=0.11mol•L-1,則反應的△H>0 | |
| C. | 相同溫度下,起始時向容器中充入1.0 molPCl5、0.20 molPCl3和0.20 molCl2,達到平衡前v(正)>v(逆) | |
| D. | 相同溫度下,起始時向容器中充入2.0 molPCl3、2.0 molCl2,達到平衡時,PCl3的轉化率小于80% |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
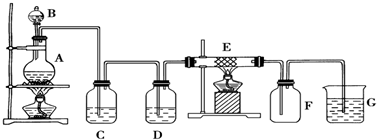
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
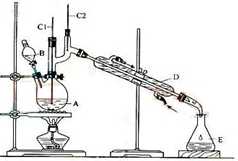 正丁醛是一種化工原料.某實驗小組利用如圖裝置合成正丁醛.
正丁醛是一種化工原料.某實驗小組利用如圖裝置合成正丁醛.| 沸點/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.72 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
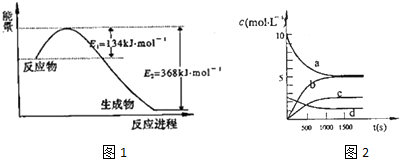
| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | x:y=3:1 | B. | v(A):v(C)=2:1 | ||
| C. | A的平衡濃度為0.4mol/L | D. | A與B的平衡濃度之比為3:2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com